Кристаллизация - твердый раствор
Cтраница 2
Разбирая процесс кристаллизации твердого раствора по диаграмме рис. 79, мы видели, что состав твердого раствора и жидкости непрерывно меняется. [16]
Пересекает объемы кристаллизации твердых растворов KI-КВг, Agl-AgBr и более сложных твердых растворов, распадающихся ниже 532 С. [17]
Пересекает объемы кристаллизации твердых растворов Na ( K) Cl ( Br) и КВг-KI. [18]
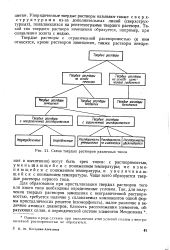 |
Схема твердых растворов различных типов. [19] |
Для образования при кристаллизации твердых растворов того или иного типа необходимы определенные условия. [20]
В температура начала кристаллизации твердого раствора непрерывно повышается. Линия ликвидуса имеет вид непрерывной кривой, все точки которой лежат между температурами кристаллизации чистых компонентов А и В. В системах второго типа ( рис. 147) температура начала кристаллизации твердого раствора понижается при добавлении одного компонента к другому. [21]
При дальнейшем отнятии теплоты начинается кристаллизация твердого раствора q, более бедного платиной, чем исходный расплав. Так как состав твердого раствора q лежит между составами твердого раствора о и жидкого раствора р, то на его образование расходуются обе эти фазы. [22]
В реальных условиях охлаждения расплава кристаллизация твердых растворов чаще всего протекает неравновесно: диффузионные процессы, необходимые для выравнивания концентрации растущих кристаллов по объему, отстают от процесса кристаллизации. В результате сохраняется неоднородность состава по объему кристалла - внутрикристаллическая ликвация: сердцевина кристаллов обогащена тугоплавким компонентом сплава, а наружные части - компонентом, понижающим температуру плавления. [24]
Для систем, в которых происходит кристаллизация твердых растворов и имеется область расслаивания, возможны различные типы диаграмм. [25]
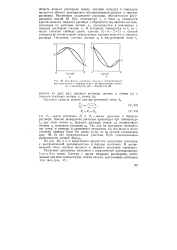 |
Диаграмма состояния системы с неограниченной растворимостью ь твердом виде с экстремальными точками с максимумом ( а и минимумом ( б. [26] |
При температуре ta в точке ап начинается кристаллизация твердого раствора и образуется двухфазная система, состоящая из расплава состава хп, находящегося в равновесии с твердым растЕюром состава хя. В интервале температур от ta до tr число степеней свободы равно единице ( С 3 - 21) п каждой температуре соответствуют определенные составы жидкого и твердого раствора. [27]
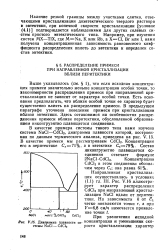 |
S. Диаграмма плавкости си - концентрации и уменьшении ско-стемы NaCl - CdCl2.. роста кристаллизации характер. [28] |
Наличие резкой границы между участками слитка, отвечающими кристаллизации доэвтектического твердого раствора и эвтектики, при конечной скорости кристаллизации ( условие (4.1) ] подтверждается наблюдениями для других солевых систем простого эвтектического типа. Например, при изучении систем MX - T1X, где MNa, К или Rb, а ХС1, Вг или I, нами получена концентрационная зависимость равновесного коэффициента распределения вплоть до эвтектики и определен состав эвтектики. [29]
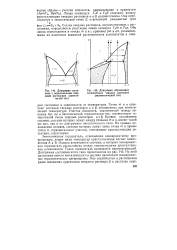 |
Диаграмма состояния с ограниченными твердыми растворами ( эвтектический тип.| Диаграмма образования. [30] |
Страницы: 1 2 3 4 5
