Кристаллизация - вещество
Cтраница 2
Кристаллизация вещества из расплава при неконтролируемых условиях обычно приводит к одновременному образованию массы мелких сросшихся кристаллов и затвердеванию расплава. Различают следующие виды такой кристаллизации: направленную, противоточную, в тонком слое и зонную плавку. [16]
Кристаллизация веществ из расплавов, особенно зонная перекристаллизация, распространена как метод получения высокочистых веществ. Ее используют на заключительных этапах очистки для удаления остаточных крайне малых количеств примесей и образования совершенной монокристаллической структуры вещества. [17]
Кристаллизацию вещества проводили в герметичном сосуде во избежание соприкосновения диметилдихлорсилана с влагой и кислородом воздуха; сосуд рассчитан на 1 - 1 5 мл вещества. [18]
Кристаллизацию вещества предлагается вызывать введением в исследуемое вещество в соответствующий момект ( за несколько градусов до кристаллизации) тонкого металлического прутика, предварительно охлажденного до температуры жидкого азота, или введени-ем в вещество в нужный момент затравки из кристаллов этого же соединения на охлажденном конце металлического прутика. [19]
Кристаллизацию вещества предлагается вызывать введением в исследуемое вещество в соответствующий момент ( за несколько градусов до кристаллизации) тонкого металлического прутика, предварительно охлажденного до температуры жидкого азота, или введением в вещество в нужный момент затравки из кристаллов этого же соединения на охлажденном конце металлического прутика. [20]
Кристаллизацию веществ проводят в кристаллизаторах - низких цилиндрических стеклянных сосудах, маточный раствор из которых можно легко удалить декантацией ( разд. [21]
Кристаллизацию веществ в процессе их очистки проводят или из раствора, или из расплава. Первый способ широко используется как одна из начальных стадий очистки солей и щелочей и относительно мало эффективен. Способы второго типа включают в себя направленную и противоточную кристаллизацию, зонную плавку, а также вытягивание из расплава. Все они базируются на постепенной кристаллизации очищаемого вещества за счет перемещения нагревательных элементов вдоль его объема. При этом примеси, для которых коэффициент распределения меньше единицы, будут обогащать жидкую часть слитка, а примеси, для которых больше единицы, концентрируются в его кристаллической части. Многократное повторение процессов плавления и кристаллизации ( от Юдо нескольких сот) приводит к накоплению примесей в головной и концевой частях слитка, составляющих около 30 % его объема. [22]
Кристаллизацию веществ в процессе их очистки проводят или из раствора, или из расплава. Первый способ широко используется как одна из начальных стадий очистки солей и щелочей и относительно малоэффективен. Способы второго типа включают в себя направленную и противоточную кристаллизацию, зонную плавку, а также вытягивание из расплава. Все они базируются на постепенной кристаллизации очищаемого вещества за счет перемещения нагревательных элементов вдоль его объема. При этом примеси, для которых коэффициент распределения меньше единицы, будут обогащать жидкую часть слитка, а примеси, для которых он больше единицы, концентрируются в его кристаллической части. Многократное повторение процессов плавления и кристаллизации ( от 10 до нескольких сотен) приводит к накоплению примесей в головной и концевой частях слитка, составляющих около 30 % его объема. [23]
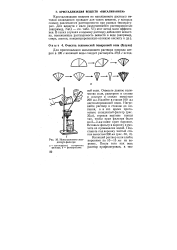 |
Использование складчатого фильтра. [24] |
Кристаллизацию веществ из насыщенного раствора методом охлаждения проводят для таких веществ, у которых сильно различаю. Для веществ с мало различающейся растворимостью ( например, NaCl - см. табл. VI) этот метод мало эффективен. [25]
Кристаллизацию веществ можно проводить из паров, расплава или раствора. В промышленности в большинстве случаев ведут кристаллизацию из раствора. Поэтому основная часть данного раздела посвящена этому виду кристаллизации. Кристаллизация из расплава, примером которой служит зонная очистка, изложена кратко. Следует отметить, что затвердевание металлов представляет собой, по существу, кристаллизационный процесс. Поэтому разработан ряд теорий, описывающих кристаллизацию металлов. Однако обсуждение этого процесса выходит за рамки настоящей работы. [26]
При кристаллизации вещества потенциальная энергия молекул уменьшается и в окружающую среду выделяется точно такое же ( по модулю) количество теплоты, что и поглощается при его плавлении. Поэтому, например, при замерзании воды массой 1 кг выделяются те же 332 кДж энергии, которые нужны для превращения такой же массы льда в воду. [27]
При кристаллизации вещества следует опытным путем подобрать соответствующий растворитель в пробирках с малым колич е-ством пробы. Температура кипения растворителя должна быть ниже температуры плавления вещества на 10 - 15 С, иначе вещество при охлаждении может выделиться в виде масла. Тогда кристалли-зацию легко вызвать трением стеклянной палочкой о стенки со-суда при сильном охлаждении смеси или растиранием капли масла в летучем растворителе ( при его сильном охлаждении), а также можно прибавить несколько кристаллов очищенного вещества в качестве затравки. [28]
При кристаллизации веществ, обладающих высокой растворимостью, следует отказаться от тепловой изоляции верхней части сепаратора, в этом случае обратный поток флегмы, образующейся при частичной конденсации пара, стекает по стенкам сепаратора и смывает осадок. В любом случае следует избегать отложений соли на границе раздела фаз пар - жидкость. Это достигается путем подбора такой скорости движения раствора и величины перегрева, при которых не возникнет бурное вскипание раствора и его разбрызгивание на входе в паровое пространство. [29]
При кристаллизации вещества из раствора оно загрязняется примесями, находящимися в исходной жидкой фазе. Следует отметить, что явление соосаждения часто используется для освобождения исходного раствора от примесей. С этой целью в раствор вводится небольшое количество специально подобранного реагента, который дает малорастворимые соединения как с примесями, так и с основным веществом. Различают истинное, гомогенное соосажде-ние и поверхностное, гетерогенное, обусловленное адсорбцией. Существенную роль в процессах соосаждения, особенно при гетерогенном соосаждении, играют условия выделения твердой фазы. При определенных условиях между твердой и жидкой фазами может быть достигнуто равновесие, в этом случае говорят о равновесном распределении примеси между указанными фазами. [30]
Страницы: 1 2 3 4