Кристаллизация - вещество
Cтраница 4
 |
Прибор для. [46] |
При кристаллизации низкоплавких веществ возможно выделение масла. Для получения кристаллов в таких случаях полезно некоторое разбавление раствора растворителем, очень медленное охлаждение и, наконец, внесение затравки. [47]
При кристаллизации низкомолокуляриых веществ отдельные кристаллич. TIC сомкнутся одна с другой; в результате весь образец оказывается полностью кристаллическим. В полимере после кристаллизации всегда сохраняются области с неупорядоченной, аморфной структурой. [48]
Процесс кристаллизации вещества из пересыщенного раствора изображается лучом кристаллизации, который соединяет точки, отвечающие составу насыщенного раствора и составу соли. Если взять насыщенный раствор, состав которого характеризуется точкой L, то луч кристаллизации для одноводного монокальцийфос-фата будет проходить по пути LN. Пересыщенные растворы расположены выше кривых FB и BD, и их составы изображаются точками, лежащими на лучах кристаллизации. Зная состав пересыщенного раствора ( например, точка Е), легко найти состав маточной жидкости после кристаллизации. [49]
Температура кристаллизации вещества постоянна и характерна для данного вещества при определенном давлении. Эта температура зависит от природы жидкой и образующейся твердой фазы. Так, сера моноклинной структуры плавится при 114 С, а ромбической структуры - при 119 С. [50]
Процесс кристаллизации вещества из расплава или раствора заключается в ориентации молекул за счет сил взаимного притяжения. Этот переход может осуществляться с различной скоростью, в зависимости от температуры, формы кристаллической решетки, строения самой молекулы, а также от степени переохлаждения раствора или расплава. Если расплав или раствор сильно переохлаждены, то кристаллизация затрудняется. [51]
Процесс кристаллизации вещества из раствора, являющийся в некотором смысле обратным процессу растворения, также сопровождается тепловым эффектом, но обратным по знаку тепловому эффекту при растворении. Количество тепла, выделяемого ( или поглощаемого) при кристаллизации единицы массы вещества ( 1 моль), называется теплотой кристаллизации. [52]
Скорость кристаллизации веществ из разбавленных титруемых растворов невелика, особенно вблизи точки стехиометричности, когда концентрации взаимодействующих ионов очень малы. Поэтому часто образуются пересыщенные растворы. [53]
Температура кристаллизации вещества постоянна и при определенном давлении характерна для данного вещества. Эта температура зависит от природы жидкой и образующейся твердой фазы. Так, сера моноклинной структуры плавится при температуре 114 С, а ромбической - при температуре 119 С. [54]
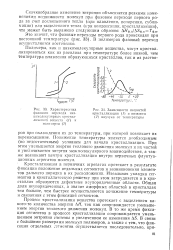 |
Характеристика фазового перехода низкомолекулярных кристаллических веществ ( 1 и полимеров ( 2.| Зависимости скоростей. [55] |
Процесс кристаллизации вещества протекает с выделением какого-то количества энергии АН, так как сопровождается уменьшением энергии теплового движения молекул. [56]
Страницы: 1 2 3 4