Кристаллизация - сульфат - натрий
Cтраница 3
При повышении температуры от 35 до 150 площадь, занимаемая на солевой проекции беркеитом, возрастает с 5 до 25 % от общей площади диаграммы в результате уменьшения объемов кристаллизации чистых сульфатов натрия и калия. Качественно новым фактом, установленным при исследовании, является изменение характера растворимости глазеритз который при 150 становится конгруэнтно растворимым соединением. [31]
На рис. 3 показана зависимость потенциала коррозии от времени и анодные поляризационные кривые экономнолегироваяннх сталей в щелочном хлоридно-сульфатном растворе при концентрации щелочи 6 г / л, что соответствует содержанию щелочи при нормальном режиме процесса кристаллизации сульфата натрия. Из рис. 3 следует, что разница между стационарным потенциалом и потенциалом активации достаточно велика ( 0 5 0 25 В), то есть все стали в таком растворе должны обладать устойчивостью к локальной коррозии. Сталь 08Х18Г8Н2Т менее устойчива к локальной коррозии ( потенциал ее активации ионами хлора более отрицателен), возможно, в связи с более низким содержанием никеля. [32]
Отработанная осадительная ванна с температурой 49 С и закрепительная ванна с температурой 58 С, стекающие с машин непрерывного процесса, смешиваются в баке-смесителе и непрерывно укрепляются при добавлении серной кислоты, сульфата цинка, поверхностно-активных веществ и маточного раствора ( после кристаллизации сульфата натрия), а также пополняются водой после промывки нити. Содержание ванны приобретает среднюю температуру 53 С и с помощью центробежных насосов фильтруется через кварцевые фильтры ( поверхность фильтрации 10 м2), а затем разделяется на осадительную и закрепительную ванны. Осадительная ванна направляется в напорные баки, откуда с температурой 51 С подается на машины непрерывного процесса; закрепительная ванна подогревается в графитовых теплообменниках до 67 С, после чего направляется в напорные баки. Из напорных баков закрепительная ванна с температурой 66 С поступает в машины непрерывного процесса; в корытах машин температура ванны поддерживается около 60 С. [33]
Производственные сточные воды образуются в результате сброса шлама при отстаивании щелочи, при диализе отжимной щелочи, мойке фильтрполотен, организованном сбросе отработанной отмывочной воды и воды из грязевых желобов прядильных машин, при мойке фильтров осадительной ванны и отделочных растворов, сбросе воды от орошения гнезд центрифуг и отжимных вальцов, сбросе охлаждающей воды при вакуум-выпарке и кристаллизации сульфата натрия, мойке оборудования и полов, а также за счет утечек и переливов растворов. [34]
Метод плавления в современных производствах сочетается с выпариванием, высаливанием и вымораживанием. Кристаллизация сульфата натрия в обогреваемых паром аппаратах тоже затруднена образованием кристаллической корки на поверхности нагрева. Как видим, вопросы кристаллизации на поверхности в производстве Na2SO4 играют существенную роль. Отложения сульфата натрия происходят не только в зоне нагрева, но и в циркуляционном контуре. Все это обусловлено способностью Na2SO4 образовывать растворы, пересыщение которых снимается сравнительно трудно. [35]
 |
Температура кипения растворов NaOH при атмосферном давлении. [36] |
При нарушениях технологического процесса содержание Na2S04 может быть значительно выше. При электролизе весь сульфат натрия переходит в электролитические щелока, поэтому при их упаривании происходит кристаллизация сульфата натрия аналогично NaCl. В связи со сравнительно низкой исходной концентрацией сульфата насыщение выпариваемого раствора по Na2S04 наступает значительно позже, чем по NaCl. При последовательном концентрировании электролитических щелоков вначале выделяются кристаллы чистой поваренной соли без примеси сульфата натрия. Естественно, что условия, при которых начинается совместное выделение кристаллов NaCl и Na2S04, зависят от исходной концентрации сульфата натрия в электролитических щелоках. [37]
Высушенный сульфат натрия автоматически взвешивается, упаковывается в мешки и направляется на склад. Показания контрольно-измерительных записывающих и регулирующих приборов вынесены на щит КИП, расположенный в отдельном помещении кристаллизации сульфата натрия. Там же размещены действующие светящиеся схемы технологического процесса кристаллизации сульфата натрия. [38]
На рис. 12 - 5 пунктиром показана изотерма системы Na, K, Cl, SO42 - - H2O при 100 С. Из рисунка следует, что при упаривании глазеритового щелока состава т, он оказывается в поле кристаллизации сульфата натрия. Следовательно, порядок выпадения солей соответствует изменению состава раствора; тенардит - тенардит галит - - тенардит галит глазерит. После отделения смеси солей раствор смешивают с сульфатным ( арка-нитовым) щелоком и вновь направляют в цикл. По первому варианту схемы получаемый после выпарки солево шлам, содержащий смесь галита и тенардита, сбрасывают в отвал. [39]
Эксплуатация оборудования пластификационной ванны не отличается от эксплуатации оборудования осадительной ванны, но, так как температура пластификационной ванны выше ( 95 - 98 С), необходимо соблюдать меры предосторожности, установленные для работ с жидкостями при высокой температуре. Это относится также к процессам, протекающим в установках контактной выпарки, к эксплуатации выпарных аппаратов осадительной ванны и кристаллизации сульфата натрия. [40]
ГДР производит - 300 тыс. т / год; мощность производства сульфата натрия на оз. Эти данные показывают, что всегда, когда есть легкодоступный хлорид натрия, предпочтительней способ высаливания и его используют вместо кристаллизации сульфата натрия за счет выпаривания растворов. [41]
Под остальными гребками мешалки ( пятым, шестым, седьмым и восьмым), которые охватывают большую часть площади муфеля, скорость реакции снова сильно замедляется. Здесь происходит окончательное образование сульфата натрия, но реакция проходит медленно вследствие наличия крупных зерен поваренной соли, комкования массы ввиду кристаллизации сульфата натрия и недостаточно высокой температуры для быстрого окончания реакции. [42]
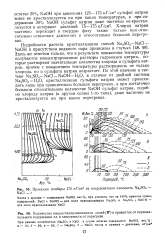 |
Проекция изобары 175 кГ / см на координатную плоскость Na2SO4 - NaCl - t.| Количества выкристаллизовавшихся солей ( W в процентах от первоначального содержания их в зависимости от перегрева. [43] |
Здесь же отметим только, что в результате повышения температуры получаются концентрированные растворы гидроокиси натрия, которые растворяют значительные количества хлорида и сульфата натрия, причем с повышением температуры растворимость не только хлорида, но и сульфата натрия возрастает. По этой причине в системе Na2SO4 - NaCl-NaOH - H2O, в отличие от двойной системы Na2SO4 - Н О, кристаллизация сульфата натрия может происходить лишь при сравнительно больших перегревах, а при достаточно большом относительном количестве NaOH сульфат натрия, подобно хлориду натрия ( и другим солям 1-го типа), даже частично не кристаллизуется ни при каких перегревах. [44]
 |
Изотермы растворимости системы H2SC4 - Na2SO4 - H2O при 0 и 25. [45] |
Страницы: 1 2 3 4