Кристаллизация - гипс
Cтраница 2
 |
Влияние температуры и содержания Р2О5 в растворе на практическую гидратированность отделяемого осадка сульфата кальция. [16] |
Необходимо, чтобы кристаллизация гипса происходила из слабопересыщенных растворов. Эти условия обеспечиваются интенсивным перемешиванием суспензии, ее рециркуляцией ( возвратом в зону загрузки исходных компонентов), предварительным смешением серной и оборотной фосфорной кислот и другими приемами. При полуги-дратном режиме экстракции, напротив, поддерживают высокие пересыщения, способствующие образованию компактных шарообразных сростков кристаллов. [17]
Необходимо, чтобы кристаллизация гипса происходила из слабопересыщенных растворов. Эти условия обеспечиваются интенсивным перемешиванием суспензии, ее рециркуляцией ( возвратом в зону загрузки исходных реагентов), предварительным смешением серной и оборотной фосфорной кислот и другими приемами. При полугидратном режиме экстракции, напротив, поддерживают высокие пересыщения, способствующие образованию компактных шарообразных сростков кристаллов. [18]
Как видим, кристаллизация гипса при твердении ангидритового вяжущего вещества имеет одну существенную особенность. Она управляется растворимостью комплекса и его прочностью. [19]
Это определяется оптимальными условиями кристаллизации гипса, рассмотренными выше. [20]
Объясняется это тем, что кристаллизация гипса сопровождается значительно меньшим расширением, чем сульфоалюмината кальция. Термодинамические расчеты и опыт показывают, что при повышении температуры, особенно при наличии в растворе ионов магния, гипс при температуре выше 40 С неустойчив, и вместо него образуется полуводный гипс или ангидрит ( 17 ], кристаллизация которых сопровождается еще меньшим увеличением объема, чем гипса. Поэтому можно предположить, что при высоких температурах и давлениях сульфатная и гипсовая агрессии для шлаковых цементов не опасны. [21]
Поэтому необходимо изыскать условия улучшения кристаллизации гипса из загрязненных фосфорнокислых растворов и ускорения их фильтрации. Одним из путей в этом направлении является осуществление экстракции фосфорной кислоты в присутствии ионов аммония, другим - раздельное выделение из раствора полу торных окислов и магнийаммонийфосфата, осажденных в опта-мальных условиях, по так называемой магнийаммонийфосфатной схеме переработки магнийсодержащих фосфоритов. [22]
В этой работе изучен процесс кристаллизации гипса при различных его начальных пересыщениях, получающихся при обменных реакциях между растворами хлористого кальция и растворами сульфатов натрия, калия и магния. [23]
На рис. 42 видны границы области кристаллизации гипса. Ее размеры весьма значительны. Вероятность выделения этой соли особенно велика из растворов, в которых много хлоридов. Преобладание ионов магния уменьшает ее незначительно, и только в присутствии избытка бикарбонатов для кристаллизации CaS04 - 2H20 требуется не менее 60 % SO в сумме анионов. Что же касается ионов кальция, то и в этом случае их достаточно в количествах 3 - 5 % в сумме катионов. [24]
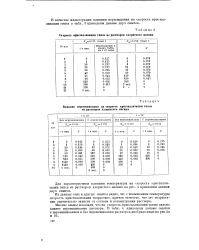 |
Скорость кристаллизации гипса из растворов хлористого магния. [25] |
Для характеристики влияния температуры на скорость кристаллизации гипса из растворов хлористого магния на рис. 4 приведены данные двух опытов. [26]
Продолжительность процесса экстракции определяется в основном условиями кристаллизации гипса, так как скорость разложения фосфатов достаточно велика. [27]
Продолжительность процесса экстракции определяется в основном условиями кристаллизации гипса, так как скорость разложения фосфатов достаточно велика. По мере расходования сильно диссоциированной серной кислоты и накопления в растворе солей и малодиссоциированной фосфорной кислоты, активность раствора и скорость процесса уменьшаются. [28]
Продолжительность процесса экстракции определяется в основном условиями кристаллизации гипса, так как скорость разложения фосфатов достаточно велика. Очевидно, что с течением времени, по мере расходования кислоты и накопления в растворе солей, скорость процесса уменьшается. На рис. 213 показана зависимость процента разложения апатитового концентрата фосфорной кислотой ( 20 % Р2О5, Т: Ж 1: 20) от времени при разных температурах. Повышение температуры увеличивает скорость разложения в начальной стадии процесса и общий процент разложения. [29]
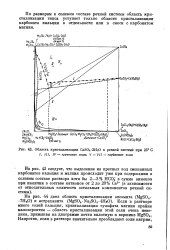 |
Область кристаллизации СаЗО ШО в речной системе при 25 С I, III, IV - грунтовые воды. V - VII - глубинные воды. [30] |
Страницы: 1 2 3 4