Кривая кристаллизация
Cтраница 1
Кривые кристаллизации пересекаются в эвтектической точке, которая соответствует одновременному насыщению обоими компонентами. Координаты эвтектической точки определяются совместным решением уравнений ( IX, 4) или графической экстраполяцией. [1]
 |
Температурная зависимость растворимости нафталина в некоторых растворителях. [2] |
Кривые кристаллизации пересекаются в эвтектической точке, она соответствует одновременному насыщению раствора обоими компонентами. [3]
Кривые кристаллизации бинарных систем делят поверхность насыщения на поля кристаллизации компонентов А, В и С ( соответственно аЕ ЕЕ, ЪЕ ЕЕъ и сЕ % ЕЕ3), над которыми находится жидкая фаза. [4]
Максимум кривой кристаллизации наблюдается при 302 4 К. Температура плавления безводной фосфорной кислоты равна 315 6 К. [5]
Если кривые кристаллизации ( или плавления) охватываются этими уравнениями, то, следовательно, они в каком-то приближении должны обладать свойствами прямоугольной гиперболы. [7]
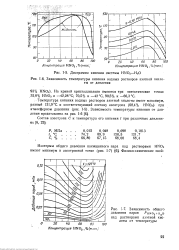 |
Диаграмма кипения системы НМО3 - Н2О.| Зависимость температуры кипения водных растворов азотной кислоты от давления.| Зависимость общего давления паров Рнмо. н о. [8] |
На кривой кристаллизации имеются три эвтектические точки: 32 8 % НМОз и - 42 28 С; 70 5 % и - 42 С, 90 5 % и - 66 3 С. [9]
Вид кривой кристаллизации и характер расплава позволяют предположить, что в системе образуется химическое соединение состава Li3Pr ( N03) 6, плавящееся инконгруентно при 282 2 С. [10]
Анализ кривой кристаллизации сульфолана показывает [25], что при 15 С наблюдается резкий изгиб кривой, указывающий на существование новой твердой фазы. Величины теплот плавления сульфолана при 26 и 15 С соответственно равны 2 73 и 10 6 кал / мол. Изомеры сульфолана с боковыми цепями, как правило, плавятся выше сульфолана. С увеличением числа углеродных атомов в боковой цепи температура плавления повышается. Замена алифатического или алициклического радикалов на ароматический приводит к резкому возрастанию температуры плавления. [11]
Метод кривых кристаллизации заключается, как мы уже отмечали ранее, в изучении изменения температуры анализируемого соединения во времени при непрерывном удалении тепла от измерительной ячейки к охлаждающей оболочке. [12]
Анализ кривых кристаллизации позволяет устанавливать не только точную температуру плавления чистого вещества, но и степень его чистоты. [13]
 |
Схематические кривые кристаллизации. а-чистого вещества ( без переохлаждения. б-несколько загрязненного. [14] |
Анализ кривых кристаллизации позволяет устанавливать не только точную температуру плавления чистого вещества, но и степень его чистоты. Нужно помнить, что для получения совершенно правильной кривой опыт следует повторять несколько раз во избежание возможных ошибок. Продолжительность всего процесса кристаллизации может быть выражена отрезком А С ( рис. 170 6); при измерении этого отрезка необходимо учитывать длительность переохлаждения и трудность установления точки С, так как в этом месте кривая обычно не имеет резкого перегиба. [15]
Страницы: 1 2 3 4 5
