Кривая кристаллизация
Cтраница 2
Метод кривых кристаллизации - изучение изменения температуры бинарной смеси во времени при непрерывном удалении ( или подводе) тепла от измерительной ячейки. В зависимости от способа удаления или подвода тепла различают статические методы - тепло подается к образцу отдельными порциями и динамические методы - непрерывный подвод или отвод тепла. [16]
На кривых кристаллизации твердых растворов могут существовать минимумы, аналогичные минимумам на диаграммах температура - состав для неидеальных растворов. [17]
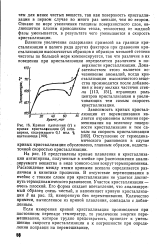 |
Кривая плавления ( 1 и кривая кристаллизации ( 2 антипирина, содержащего 0 1 мол. % ацетанилида. [18] |
Если измерения кривой кристаллизации производятся при постоянном перепаде температур, то увеличение энергии перемешивания, которое трудно предотвратить, приведет к уменьшению скорости кристаллизации и к погрешности при определении поправки на перемешивание. [19]
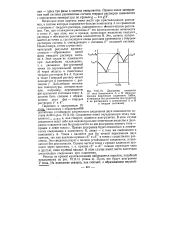 |
Диаграммы плавкости IV типа [ компоненты А и В образуют прочное химическое соединение AnBm, плавящееся без разложения ( конгруэнтно и не растворимое в компонентах А и В в твердом состоянии ]. [20] |
Иногда на кривой кристаллизации наблюдается перелом, подобный показанному на рис. VIII. [21]
Пологий ход кривой кристаллизации NaF указывает на тенденцию к расслаиванию. [22]
 |
Пути кристаллизации в трехкомпонентной системе с бинарными твердыми растворами. [23] |
По достижении кривой кристаллизации эвтектической линии в h происходит одновременное насыщение расплава кристаллами компоненты А и смешанными кристаллами состава За. [24]
Неудобство метода кривых кристаллизации по сравнению с кривыми плавления, а именно наличие переохлаждения, в ряде случаев удастся свести к минимуму, а иногда и уничтожить полностью с помощью охладительной иглы. [25]
Переохлаждение на кривых кристаллизации часто удается свести к минимуму, а иногда и уничтожить полностью с помощью охладительной иглы. [26]
Каждая из кривых кристаллизации выражает связь между температурой и концентрацией раствора, равновесного с кристаллами данного вида. Каждую из этих двух переменных принимать в качестве независимой, зависит только от постановки вопроса. Каждая такая кривая может быть использована и для выражения зависимости температуры кристаллизации от концентрации раствора и, наоборот, для выражения зависимости концентрации раствора, равновесного с данными кристаллами, от температуры. В последнем случае эти кривые могут рассматриваться как кривые растворимости. Правая кривая рис. 21 выражает растворимость нитрата калия при разных температурах, а левая - растворимость льда в растворах нитрата калия. [27]
Изучение хода кривых кристаллизации показывает наличие определенных вариаций состава кордиерита и образование здесь твердых его растворов. [28]
После получения кривых кристаллизации образца на шкале прибора с минимальной чувствительностью из наклона площадки видно, имеет ли смысл производить запись ее на шкале с большей чувствительностью. Так, кривые кристаллизации веществ, содержащих свыше 1 % примеси, нет смысла записывать с точностью, превышающей 0 1, кривые веществ, содержащих до 0 1 % примеси, следует записывать с точностью до сотых долей градуса, более чистые вещества - с максимальной точностью. Наличие самописца, позволяющего производить запись кривых с различной точностью, важно и для других работ, связанных с необходимостью записывать и обрабатывать любые кривые время - температура. [29]
Так как на кривой кристаллизации 1 - 2 из жидкости непрерывно выделяется свинец, то жидкость по мере кристаллизации свинца обогащается сурьмой. [30]
Страницы: 1 2 3 4 5