Спонтанная кристаллизация
Cтраница 2
Получение при спонтанной кристаллизации прозрачного однофазного материала свидетельствует об очень малой энергии нуклеации и очень высокой кристаллизационной способности. И то, и другое вполне возможно в области образования твердых растворов, так как здесь не требуется работы диффузии, а должно иметь место, по-видимому, не связанное с диффузией упорядочение, ведущее к переходу из стеклообразного состояния в кристаллическое с выпадением твердых растворов. [16]
Сравнительно недавно возможность спонтанной кристаллизации отрицалась вообще. Любой раствор, будь он пересыщен или нет, содержит определенное количество растворимых и нерастворимых примесей, которые оказывают влияние на кинетику фазового превращения. Нерастворимые примеси могут стать центрами кристаллизации и тем самым, как предполагалось, исключить спонтанное образование зародышей. Дальнейшие исследования над пересыщенными растворами [24-28] показали, однако, что возникновение частиц новой фазы может происходить как самопроизвольно, так и на уже готовой твердой поверхности. Но роли посторонней поверхности в процессе образования кристаллов придается очень большое значение. Согласно Фольмеру [4] и Френкелю [2], образование зародышей на готовой поверхности происходит легче, чем в объеме раствора, потому что работа их образования на границе раздела фаз меньше работы, требующейся для возникновения зародыша в объеме раствора. [17]
Моделью этого процесса является спонтанная кристаллизация, когда вокруг флюктуационно возникшего скопления молекул одного антипода начинается избирательная кристаллизация. [18]
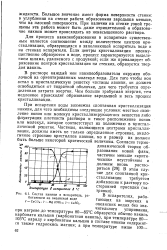 |
Состав накипи в испарителе, работающем на океанской воде / - СаСО3. 2 - Mg ( OHh. 3 - CaSO4. [19] |
При испарении воды возможна спонтанная кристаллизация накипи, для чего необходимы следующие условия: местное скопление ионов или молекул кристаллизирующегося вещества либо флуктуация плотности раствора и такое расположение ионов или молекул, которое соответствует их положению в кристаллической решетке. Частицы, являющиеся центрами кристаллизации, должны иметь не только определенное строение, аналогичное строению кристаллов накипи, но и размер их должен быть больше некоторой критической величины. [20]
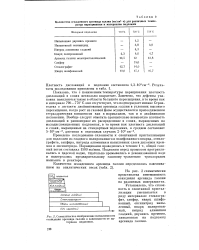 |
Схематическое изображение интенсивности J r. [21] |
Проведено исследование склонности к спонтанной кристаллизации для подложек из гладкого полированного и шлифованного кварца, стекло-графита, сапфира, нитрида алюминия и напыленных слоев двуокиси кремния и оксинитрида. Наращивание проводилось в течение 1 ч, общий газовый поток составлял 1500 мл / мин. Подложки перед процессом протравливались в царской водке, тщательно промывались в деионизованной воде и подвергались предварительному газовому травлению трихлоридом мышьяка в реакторе. [22]
 |
Графики изменения во времени количества алмазной ( С & ( 1, 2 к перекристаллизованной графитовой ( Сг ( 3 фаз при Р 5 4 ГПа, Г1470 К в реакционных объемах 0 7 - IO - м3 ( I и 3 5 Ю-6 м3 ( 2, 3. [23] |
Ограничение длительности процесса алмазообразования при спонтанной кристаллизации может быть обусловлено различными причинами, например, неконтролируемыми изменениями р - Т - условий процесса, в частности, снижением давления при образовании из графита более плотного алмаза; появлением в реакционной зоне фаз, конкурирующих с ростом алмаза. Как отмечалось, такой фазой является монокристаллический графит. С целью выяснения его роли в процессе кристаллизации алмаза была проведена ( в камерах с реакционным объемом 3 5 10 - 6 м3) специальная серия экспериментов, которая обеспечила получение для последующего изучения трех групп образцов. К первой отнесены пробы графита с поверхности его контакта с расплавом металла, свободной от алмаза. Ко второй - слои металла преимущественно в виде пленок толщиной от 5 - 10 - 5 до 8 - 10 - 4 м, отделявшие алмаз от источника углерода, одна сторона которых являлась отпечатком с поверхности граней алмаза, а противоположная сторона представляла собой границу металл - графит. [24]
Относительное пересыщение, необходимое для спонтанной кристаллизации, помимо прочих условий, существенно зависит от формулы соединения. В то время как при осаждении сульфата бария для образования зародыша необходимо как минимум два иона, минимальное число ионов для квасцов и нитрата хрома равно четырем, а в случае фосфата бария их даже пять, что значительно снижает вероятность зародышеобразования. [25]
Сообщалось [26] и об осуществлении спонтанной кристаллизации только одной хиральной формы кристалла, но повторение таких спонтанных кристаллизации в условиях, в которых заведомо исключено случайное внесение зародыша кристаллизации, должно привести статистически к выпадению в осадок с равной вероятностью как одной, так и другой кристаллической формы. Это не означает, что в одном кристаллизаторе будет находиться равное количество () - и ( -) - кристаллов, так как может иметь место явление аутокристаллизации. Соре [59] проводил 938 раз в запаянных ампулах спонтанную кристаллизацию хлората натрия, молекулы которого ахиральны, но образуют хиральные кристаллы. Правовращающие кристаллы выпадали в 433 случаях, лево-вращающие - в 411 случаях, и смесь обеих форм выпадала 94 раза. [26]
 |
Графики изменения во времени количества алмазной ( Са ( /, 2 и перекристаллизованной графитовой ( Сг ( 3 фаз при Р 5 4 ГПа, Г1470 К в реакционных объемах 0 7 - IO - м3 ( 1 и 3 5 Ю-6 м3 ( 2, 3. [27] |
Ограничение длительности процесса алмазообразования при спонтанной кристаллизации может быть обусловлено различными причинами, например, неконтролируемыми изменениями р - Т - условий процесса, в частности, снижением давления при образовании из графита более плотного алмаза; появлением в реакционной зоне фаз, конкурирующих с ростом алмаза. Как отмечалось, такой фазой является монокристаллический графит. С целью выяснения его роли в процессе кристаллизации алмаза была проведена ( в камерах с реакционным объемом 3 5 10-в м3) специальная серия экспериментов, которая обеспечила получение для последующего изучения трех групп образцов. К первой отнесены пробы графита с поверхности его контакта с расплавом металла, свободной от алмаза. Ко второй - слои металла преимущественно в виде пленок толщиной от 5 - 10 - 5 до 8 - 10 - 4 м, отделявшие алмаз от источника углерода, одна сторона которых являлась отпечатком с поверхности граней алмаза, а противоположная сторона представляла собой границу металл - графит. [28]
Предельные пересыщения определяются по началу спонтанной кристаллизации в перемешиваемом [8, 9] или неперемешиваемом [10] пересыщенном растворе, в присутствии или отсутствие затравки. [29]
Кристаллизационная способность стекол измеряется скоростью их спонтанной кристаллизации и линейной скоростью роста кристаллов. Она является одним из важных технологических свойств стекла и часто определяет Практическую возможность изготовления стекла данного состава. Обычно кристаллизационную способность характеризуют величиной линейной скорости роста кристаллов, образующихся в стекле данного состава, в определенных температурных интервалах. Естественно, что величина кристаллизационной способности зависит и от того, каковы природа и химический состав выпадающих кристаллов. [30]
Страницы: 1 2 3 4