Равновесная кристаллизация
Cтраница 5
Из изложенных общих соображений о равновесных ( обратимых) процессах понятно, почему мы применяем термин равновесная кристаллизация, понимая под ней направленную кристаллизацию в однородном концентрационном поле расплава. Такая кристаллизация протекает при 1 / Уг. Концентрационное поле расплава по мере направленной кристаллизации изменяется, но скорость исчезновения возникающих при этом возмущений концентрационного поля меньше Vr. [61]
 |
Диаграмма состояния системы SiO Na2SiO - PbSiOj. [62] |
На полях кристаллизации Na2O 2SiO2 и силиката Na2O: ЗРЬО 6SiO2 пунктирными линиями выделены ресорбционные области соединений / и VI, для которых равновесная кристаллизация происходит с полной ресорбцией первичной фазы. [63]
А в нем после разделения суспензии ( кристаллизата); К, Ск - выход кристалли-яеского продукта и концентрация компонента А в нем при равновесной кристаллизации; М, См - количество захваченной маточной жидкости и концентрация компонента А в ней. [64]
Кривые АЕ j, EJDEz, E2PF и РВ называются линиями ликвидуса ( от латинского слова liquidus - жидкость); они характеризуют температуры начала равновесной кристаллизации. Следует отметить, что на изотермических диаграммах линии ( на плоскости) и поверхности ( в объеме) ликвидуса обычно характеризуют составы насыщенных растворов ( растворимости) отдельных веществ. Линии и поверхности солидуса ( solidus - твердое тело) выражают составы отдельных твердых фаз. [65]
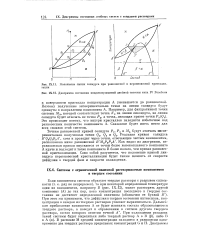 |
Положение линии солидуса при равновесной и неравновесной кристаллизации.| Диаграмма состояния конденсированной двойной системы типа IV Розебома. [66] |
Как видно из диаграммы, неравновесная кривая опускается от точки более высокоплавкого компонента А круче и подходит к точке компонента В более полого, чем кривая равновесной кристаллизации. Само собой разумеется, что положение кривой ликвидуса неравновесной кристаллизации будет также зависеть от скорости диффузии в твердой фазе и скорости охлаждения. [67]
Страницы: 1 2 3 4 5