Металлический атом
Cтраница 2
Заметим, что у изолированного металлического атома ( состояние одноатомного пара, возникающее при высоких температурах и высоких степенях разрежения) окислительно-восстановительные свойства характеризуются другой величиной, называемой ионизационным потенциалом. Ионизационный потенциал - это энергия, необходимая для отрыва электрона от изолированного атома. [16]
Однако комплексы, в которых металлический атом образует две V-образных связи, по-видимому, встречаются редко. Однако такие комплексы до настоящего времени еще не были выделены. [17]
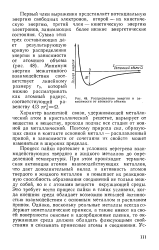 |
Распределение энергии в зависимости от атомного объема. [18] |
Характер валентной связи, удерживающей металлический атом в кристаллической решетке, варьирует от вещества к веществу, проходя подчас все стадии от ионной до металлической. Поэтому природа сил, образующих связи в контакте основной металл - расплавленный припой, в зависимости от сочетания их свойств может изменяться в широких пределах. [19]
При одинаковом повышении формальной валентности металлического атома отрицательная свободная энергия образования его гидратного комплекса уменьшается, как правило, сильнее, чем пересчитанная на тот же атом энергия образования окисла. [20]
Таким образом, процесс образования металлических атомов из водных растворов эн-дотермичен и требует определенного времени и значительной энергии. [21]
 |
Структура TISe. [22] |
Аналогичные случаи наблюдаются п у металлических атомов. Так, в соединении PbS свинец имеет формальную валентность 2, и, следовательно, в связи участвует только два из четырех валентных электронов. Эти факты позволяют сделать заключение о том, что Т1Г одновалентен, а Т1ц - трехвалентен. Следовательно, атомы Т1Г не используют двух своих валентных электронов. [23]
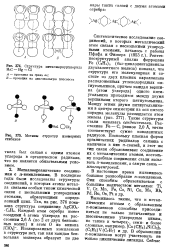 |
Структура метилмеркурхлорида Н3С - Hg - С1.| Мотивы структур изомерных стибинов. [24] |
Выяснилось также, что к металлическим атомам с образованием я-комплексов способны присоединяться не только пятичленные и шестичленные углеродные циклы, но также и четырех -, семи - и более сложные, например, [ Си ( СНз) 4 № СЬ ] 2, ( CsHsJV CrH. В образовании я-комплексов могут участвовать не только циклические лиганды. [25]
 |
Структура пальмиерита К2РЬ - ( SOib ( белыми кружками обозначены ионы калия.| Структура гипса CaSCU. [26] |
Значительно реже центром комплексного аниона являются металлические атомы, хотя для некоторых из них это характерно. [27]
При этом предполагалось, что система металлических атомов в процессе поглощения азота остается неизменной. Это допущение, однако, справедливо лишь для четырех указанных выше металлов с атомными радиусами, превышающими 1 73 А. [28]
Силициды с металлическими структурами образованы замещением металлических атомов атомами кремния без перестройки решетки металла ( иногда с уплотнением), при котором наряду с металлическими связями между атомами имеются ковалентные. [29]
Способность у - АЬОз проводить стабилизацию металлических атомов, Образовывать на своей поверхности запасы молекулярных и хе-мосорбированных форм электронодонорных газов ( СО и На), оказывать решающее влияние на энергию их связи с поверхностью металлических контактов приводит к увеличению на порядок удельной активности металлов на этом носителе в реакции окисления СО [ 10J п - сравнению с другими носителями. Необходимо синтезировать низкопроцентные катализаторы ( до 0 5 вес. [30]
Страницы: 1 2 3 4