Кинетический критерий
Cтраница 3
Непосредственное наблюдение образования ацильным соединением тетра-эдрического продукта присоединения еще не является убедительным доказательством, что это или подобное промежуточное соединение действительно возникает на пути данной реакции, так как оно может возникнуть и в результате побочного процесса. Кинетические критерии обладают тем преимуществом, что позволяют установить существование промежуточного продукта на основном пути реакции, так как наличие побочной реакции не должно оказывать влияния на кинетику до тех пор, пока не станет заметной убыль исходных веществ в результате образования большого и легко определяемого количества побочного продукта. [31]
 |
Относительные скорости сольволиза аллильных хлорпроизводимх. [32] |
Большая часть данных, касающихся аллильной SNl реакционной способности, взята из работ по изучению сольволиза аллильных галогенпроизводных, которые будут обсуждаться ниже. Кинетический критерий молекулярности реакции обычно не приложим к реакциям сольволиза, но все же можно воспользоваться некоторыми экспериментальными данными по скорости SN2 реакций галогенпроизводных с растворителем. Когда растворитель имеет низкую нуклеофильность наряду с высокой ионизирующей способностью, как в случае концентрированного водного раствора муравьиной кислоты, меньше вероятность появления усложняющих факторов. [33]
 |
Относительные скорости сольвошша аллильных хлорпроизводиых. [34] |
Большая часть данных, касающихся аллильной SNi реакционной способности, взята из работ по изучению сольволиза аллильных галогенпроизводных, которые будут обсуждаться ниже. Кинетический критерий молекулярности реакции обычно не приложим к реакциям сольволиза, но все же можно воспользоваться некоторыми экспериментальными данными по скорости SN2 реакций галогенпроизводных с растворителем. Когда растворитель имеет низкую нуклеофильность наряду с высокой ионизирующей способностью, как в случае концентрированного водного раствора муравьиной кислоты, меньше вероятность появления усложняющих факторов. [35]
Предлагается следующий кинетический критерий: на основе гипотетической структуры должен быть возможен вывод кинетического уравнения, описывающего экспериментально наблюдаемую кинетику. [36]
Наличие в схеме быстрых обратимых стадий, связанных, например, с комплексообразованием, может приводить к зависимости наблюдаемой энергии активации от температуры. Появление отрицательных значений энергии активации может рассматриваться как кинетический критерий участия молекулярных комплексов в химическом процессе. [37]
Если учесть, что электрофильности бромной ртути недостаточно для осуществления обмена, то в присутствии бромид-иона, когда возможно образование комплекса HgBrs, в котором резко понижены электрофильные свойства агента, трудно ожидать осуществления механизма 5.2 - типа. Таким образом, этот пример еще раз показывает недостаточность одного кинетического критерия для суждения о механизме реакции. [38]
Свободно-радикальный механизм дает чрезвычайно гибкую систему для получения огромного разнообразия продуктов реакции. Именно по этой причине иногда считают, что такой механизм слишком неспецифичен и не поддается обычной проверке по кинетическим критериям. Могут сказать также, что он объясняет слишком многое. Это возражение, однако, вряд ли относится к настоящему примеру. Мы постулируем не совокупность неразличимых свободно-радикальных реакций в гомогенной фазе, а лишь объясняем весьма необычную реакционную способность в организованной макромолекулярной системе, которую вряд ли можно объяснить с точки зрения чистой геометрии. Возможно, что перемещение свободных валентностей по всей системе структур дает особый вид реакционной способности, и постоянное наличие свободных валентностей или же возможность их возникновения является одной из основных характерных особенностей живого вещества. [39]
Если же условие независимости реакционных групп не выполняется, то реализуется необходимое условие возникновения осцилляции скорости реакций: один и тот же промежуточный компонент ( концентрация которого не задана внешними условиями) выполняет в схеме реакции две или более различные функции. В этом случае условием устойчивости стационарного состояния, если таковое, конечно, возможно при данных внешних условиях, определяется кинетическим критерием устойчивости, основанным на анализе малых отклонений от стационарного режима. [40]
В последние годы многое сделано но исследованию механизма инги-бирующего действия фосфитов. Были идентифицированы кинетические отдельные элементарные стадии, проанализированы скорости обрыва цепей и подавления вырожденного разветвления при ингибированном фосфитами окислении полимеров, а также сформулированы кинетические критерии появления синергических эффектов при добавках к ингибиторам вторых компонентов. [42]
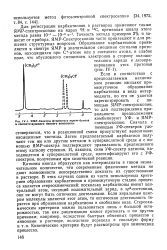 |
ПМР-Спектры фтористого mp. m - бутила КОМбиНИРУЮТ УФ - И ЯМР-и соответствующего ионного комплекса. СПбКТрОСКОПИЮ. Сначала С. [43] |
Катионы иногда образуются как интермедиаты в таком незначительном количестве, что современные физические методы не дают возможности непосредственно доказать их существование в растворе. Если хиральным центром молекулы является этот атом, то оптическая деятельность теряется при образовании карбкатиона в свободном виде. Кинетические критерии будут рассмотрены при химических процессах. [44]
На основании вида формально-кинетического уравнения, описывающего скорость гидролиза erop - бутилсульфат-иона в щелочной среде, этот процесс следовало бы отнести к Sjyi-типу. Рассмотрение же стереохимии реакции приводит к выводу о 5 2-механизме замещения. Однако кинетический критерий не учитывает участия растворителя в процессе реакции, и наблюдаемая реакция является лишь псевдомономолекулярной, о характере переходного состояния которой ничего определенного сказать нельзя. Поэтому установление мономолекулярности процесса не может быть достаточным условием для вывода об образовании в медленной стадии карбка-тиона, как это должно быть в случае истинного 5 1 -замещения. [45]
Страницы: 1 2 3 4