Аминокислота - даюта
Cтраница 1
Аминокислоты дают с нингидрином интенсивное окрашивание, которое может быть использовано для их количествен-ного определения. Приводим ее здесь с небольшими изменениями, предложенными Е. Т. Коссовой, применительно к цельной крови. [1]
Аминокислоты дают с медью и некоторыми другими тяжелыми металлами окрашенные внутренние, или хелатные, комплексные соли, очень трудно растворимые и устойчивые. Так, комплекс меди с гликоколем окрашен в темно-синий цвет и не разлагается едким натром, а только сероводородом. Аминокислоты образуют аналогичные, но менее стойкие комплексы; у - и S-аминокислоты не образуют подобных соединений. [2]
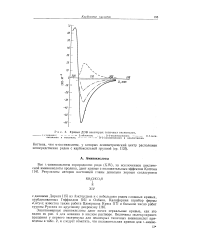 |
Кривые ДОВ некоторых типичных оксикислот. [3] |
Энантиомерные аминокислоты дают почти зеркальные кривые, как это видно из рис. 4 для аланина в кислом растворе. [4]
Наимоноиания аминокислотам дают но тем кислотам, производными которых они являются. [5]
С минеральными кислотами аминокислоты дают соли, подобно аминам. [6]
Недавно опубликованные мною опыты18 по образованию альдегидов из аминокислот дают некоторые указания на значение кислорода для действия фермента. При реакции Штрекера акцептор водорода ( аллоксан, бензохинон) постепенно восстанавливается освобождающимся при расщеплении воды водородом. Начало реакции не зависит от присутствия или отсутствия кислорода. Только после полного восстановления акцептора водорода начинается действие кислорода, который окисляет восстановленный акцептор с возрождением первоначального соединения ( гидрохинон в хинон) и роль которого для дальнейшего хода реакции является решающей. Что кислород необходим уже в начале действия тирозиназы, объясняется тем, что этот фермент не содержит готового акцептора водорода атмосфере водорода не происходит ни малейшего превращения тирозина под действием тирозиназы, в то время как при равных условиях расщепление аланина бензохиноном легко доказать. Наиболее соответствует фактам то предположение, что под влиянием кислорода образуется акцептор водорода, который попеременно восстанавливается водородом воды и окисляется свободным кислородом ( вероятно, при содействии фенолазы) и обусловливает гидролитическое окисление тирозина. [7]
Вторую группу составляют белки, которые при гидролизе помимо аминокислот дают и другие компоненты. Неаминокислотная часть сложного белка именуется простетической группой, по которой и осуществляется классификация таких белков. [8]
Аммиак и газообразная СО2 могут соединяться с образованием аммонийной соли карбаминовой кислоты; подобным же образом, аминокислоты дают при взаимодействии с газообразной СО2 карбамино - ( N-карбоксиамино) кислоты. Их кальциевые соли растворимы в воде и нерастворимы в этиловом сшрте. Простое кипячение с водой регенерирует исходные аминокислоты. [9]
Простыми называют белки, которые при гидролизе распадаются исключительно на аминокислоты; сложными - белки, которые при гидролизе наряду с аминокислотами дают соединения другого характера, например нуклеиновые кислоты, углеводы, фосфорную кислоту и пр. Сложные белки, или протеиды, состоят, таким образом, из собственно белковой части в сочетании с другими, небелковыми веществами. [10]
Первой стадией метаболизма 2 4 - Д в растениях является гидроксилирование с образованием 4-гидрокси - 2 3 - или 4-гидрокси - 2 5-дихлорфеноксиуксусных кислот [8], которые с углеводами и аминокислотами дают достаточно стабильные конъюгаты, способные длительное время сохраняться в растениях без существенных изменений. [11]
С минеральными кислотами аминокислоты дают соли подобно аминам. [12]
С минеральными кислотами аминокислоты дают соли, подобно аминам. [13]
Первичная аминогруппа а-аминокислот типа RCH ( NH3) CO2 - обладает всеми характерными реакциями этой группы ( разд. При взаимодействии с минеральными кислотами аминокислоты дают соли, хотя фактически это протонированныйг карбоксилат-анион цвиттер-иона. Обработка азотистой кислотой приводит к соответствующим гидроксисоединениям. [14]
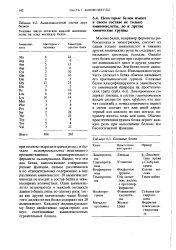 |
Сложные белки. [15] |
Страницы: 1 2