Аминокислота - даюта
Cтраница 2
Многие белки, например ферменты ри-бонуклеаза и химотрипсин, состоят из одних только аминокислот и никаких других химических групп не содержат; их называют простыми белками. Однако есть белки, которые при гидролизе помимо аминокислот дают и другие химические компоненты. [16]
Фишера ( 1901 г.) состоит в этерифи-кации аминокислот метанолом и дробной перегонке эфиров. Результаты далеко не количественны, так как в лучшем случае определенные таким образом аминокислоты дают лишь 60 - 70 % общего количества азота, содержащегося в белке. [17]
Белки представляют собой высокомолекулярные азотсодержащие вещества природного происхождения, в состав которых в качестве основных звеньев входят аминокислоты. Те белки, которые построены из одних только аминокислот, носят название протеинов или простых белков, те же, которые при расщеплении помимо аминокислот дают и молекулы, не являющиеся аминокислотами, например фосфорную кислоту при расщеплении казеина, пурин и пиримидинфосфорнокислые эфиры Сахаров при расщеплении нуклео-протеидов, обозначаются как сложные белки или протеиды. Новейшие исследования показали, что такое деление вряд ли является правильным, потому что большинство белковых веществ содержит наряду с аминокислотами и другие составные части; протеины же в точном смысле слова встречаются чрезвычайно редко. [18]
В качестве группового локализующего агента применяется 0 25 % - ный ( масс. / об.) раствор нингидрина в ацетоне. Пятна можно проявлять нагреванием при 100 С в течение 5 мин или с целью получения более светлого фона выдерживанием при комнатной температуре в течение нескольких часов. Аминокислоты дают пурпурные пятна; гистидин и глицин красно-серые; фенилаланин, тирозин и аспарагиновая кислота синие; триптофан коричневые; аспарагин грязно-желтые; пролин желтые. Чувствительность варьирует в диапазоне от 0 2 мкг для глицина до 2 мкг для гистидина. [19]
Хроматограмму опрыскивают 0 2 % - ным раствором изатина в н-бутаноле, содержащем 4 % уксусной кислоты. Прогревают при 105 С в течение 15 мин. Многие аминокислоты дают окраску в этом же диапазоне цветов, которая исчезает при комнатной температуре через несколько часов. [20]
Они представляют собой кристаллические твердые вещества, плавящиеся при относительно высоких температурах ( с разложением), растворимые в воде, но не растворимые в этаноле и других органических растворителях. Некоторые ароматические аминокислоты обладают небольшой растворимостью в воде, но легко растворяются в разбавленной кислоте или щелочи. С ацетатом меди аминокислоты дают медные соли, которые плохо растворимы в воде. Реакция водного раствора аминокислоты может быть нейтральной, щелочной или кислой в зависимости от соотношения амино - и карбоксильных групп, присутствующих в молекуле. [21]
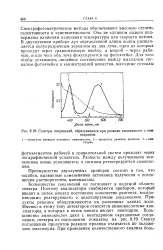 |
Спектры соединений, образующихся при реакции аминокислот с нин. [22] |
Большинство соединений не поглощает в видимой области спектра. Поэтому анализаторы снабжаются прибором, который вводит в поток элюата постоянное количество реагента, воспроизводимо реагирующего с анализируемым соединением. Продукты реакции обнаруживаются на различных длинах волн. Именно к этому типу детекторов относятся аминокислотные анализаторы, в которых в поток элюата вводят нингидрин. Большинство аминокислот дают с нингидрином окрашенные соединения; спектры их поглощения показаны на рис. 8.19. Спектр поглощения продуктов реакции пролина отличается по положению максимума. [23]
 |
Круговорот азота. Азот составляет 79 % объема атмосферы - главного резервуара этого элемента. [24] |
Большинство растений в качестве источника азота используют нитрат-ионы. Животные в свою очередь прямо или косвенно получают усвояемый азот из растений. На рис. 10.11 показано, как образуются нитраты после разложения белка мертвых тканей сапротрофными бактериями и грибами. Этот процесс включает окислительные реакции с участием кислорода и аэробных бактерий. Белки сначала расщепляются до аминокислот, а затем аминокислоты дают аммиак. Этот же продукт образуется при разложении экскретов и фекалий животных. [25]
Каждая аминокислота дает пик, близкий к гауссову распределению. Иминокислоты ( пролин, гид-роксипролин) дают производные, у которых максимум поглощения лежит при 440 нм; следовательно, необходим дополнительный спектрофотометр с выходом на второй конец самописца. Площади пиков можно определять вручную или же вводить данные либо в интегратор, либо в небольшую вычислительную машину. Кроме того, раствор содержит восстанавливающий агент, такой как хлорид олова ( II) или гидринданхин. Последний предотвращает побочные окислительные процессы, которые влияют на точность анализа. Аминокислоты дают несколько различающиеся спектрофотометрические выходы, поэтому для проверки точности анализа всегда используют стандартную смесь аминокислот. Чувствительность анализа примерно 1 нмоль. Сделаны попытки повысить чувствительность с помощью спектрофлуорометрических методов анализа. Одним же из потенциальных реагентов является 4-фенилспиро [ фуран-2 ( ЗЯ), l - фталан ] дион-3 3 ( 3) ( флуореска-мин), который не флуоресцирует. Последние возбуждаются при 390 нм и имеют максимум поглощения при 475 нм. Несмотря на то, что относительное повышение чувствительности по сравнению со спектрофотометрическими методами на первый взгляд выглядит привлекательным, реагент ( 3) весьма дорог, а аминокислоты не дают флуоресцирующих продуктов до тех пор, пока величина рН кислого элюата не будет доведена до необходимого значения. Альтернативным реагентом для спектро-флуорометрии является о-фталевый ангидрид, однако он также обладает двумя упомянутыми недостатками. [26]
Амины можно подвергать диазогированию и сочетанию. Для открытия соединений, способных сочетаться с солями диааония, эта реакция может быть использована при хроматографировании с таким же успехом, как при колориметрировании. Эстрон, эстрадиол и эстриол были разделены после сочетания с солью диазония. Для разделения Сахаров ( и стеринов) была использована хроматография эфиров n - фенилазобензойной кислоты. Метиловые эфиры аминокислот были разделены методом хроматографической адсорбции N-азобензол-я - сульфонильных производных на окиси алюминия, обработанной 10 % - ным раствором уксусной кислоты в метиловом спирте. Холевая и дезоксихолевая кислоты были разделены после этерификации с помощью w - бром-я-метилазобензола. Этиловые эфиры аминокислот дают с азобензол-п-изоцианатом окрашенные производные, разделяющиеся на окиси алюминия. [27]
Страницы: 1 2