Контурная диаграмма
Cтраница 1
 |
Изменение энергетического состояния реагирующей системы ( контурная диаграмма. [1] |
Контурная диаграмма по своему построению сходна с изображением рельефа я а географических картах. [2]
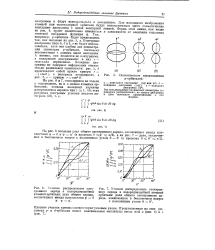
Контурные диаграммы типа 5, б и 5, в не будут использоваться, хотя они удобны для демонстрации симметрии р-орбитали, поскольку несовместимы с данным в шге описанием. А именно, они являются не контурными, а полярными диаграммами; в них г - зависимая переменная. [4]
Контурные диаграммы орбиталей ( 188) даны на рис. 17 для сравнения с исходными а - и я-орбиталями. [5]
Контурные диаграммы орбиталей ( 188) даны на рис. 17 для сравнения с исходными а - и л-орбиталями. [6]
Контурные диаграммы орбиталей основаны на эскизах, приведенных в книге Jorgensen W. J., Salem L. Имеется несколько более поздних расчетов, однако для наших целей контурных диаграмм Йоргенсена и Салема более чем достаточно. [7]
Контурные диаграммы молекулярных орбиталей, примеры которых были даны в главе 1 ( рис. 1.15 - 1.22), получены в результате компьютерного расчета. Они дают объемные представления о пространственной форме орбиталей, которая характеризует распределение плотности данной занятой или данной незанятой орбитали по отдельным атомам молекулы, т.е. вклад каждой атомной орбитали в рассматриваемую МО. Суммируя вклады АО отдельных атомов по всем связывающим МО, мы получаем картину распределения электронной плотности в молекуле. Распределение плотности граничных орбиталей ВЗМО и НСМО дает представление о преимущественном месте атаки электрофилов или нуклеофилов, т.е. об ориентации в реакциях присоединения или замещения с участием данной молекулы. [8]
 |
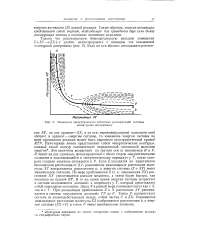
Контуры зарядовой изоплотности для репульсивного основного состояния молекулы Ве2 ( а и контуры зарядового натекания и вытекания для того же состояния Ве2 ( б. [9] |
Контурные диаграммы распределения плотностей дают многое для понимания молекул и наглядны, так же как и условные геометрические радиусы атомных орбиталей. Однако следует помнить, что и для атомов химическое поведение больше зависит не от геометрии, а от потенциалов ионизации и возбуждения, а также от поляризуемости электронных облаков. [10]
Из контурной диаграммы для синглетного состояния видно, что те конфигурации, в которых оба электрона находятся по одну сторону от ядра, преобладают, тогда как по контурной диаграмме для триплетного состояния видно, что преобладают конфигурации, имеющие электроны по разные стороны от ядра. В действительности, электроны с одинаковым спином будут иметь максимум вероятности нахождения по разные стороны от ядра на прямой линии, проходящей через ядро т.е. под углом в 180 по отношению друг к другу. Как нетрудно заметить, тот же самый результат был получен ранее при гибридизации атомных s - и р-орбиталей с образованием двух эквивалентных гибридных sp - орбиталей. Единственное отличие здесь в том, что в данном случае рассматривались атомные конфигурации Is12p1, а не nsinp1, которые необходимы для образования эквивалентных гибридных орбиталей. Однако это было сделано только для простоты изложения. Угловая корреляция, которая будет рассмотрена далее, не зависит от того, имеют или не имеют s - и р-орбитали одно и то же главное квантовое число. [11]
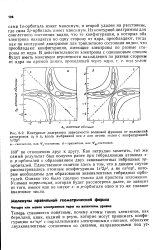 |
Контурные диаграммы зависимости волновой фуниции от положений электронов Zi и z2 вдоль выбранной оси г для атома гелия с конфигурацией. [12] |
Из контурной диаграммы для синглетного состояния видно, что те конфигурации, в которых оба электрона находятся по одну сторону от ядра, преобладают, тогда как по контурной диаграмме для триплетного состояния видно, что преобладают конфигурации, имеющие электроны по разные стороны от ядра. [13]
Из контурной диаграммы для синглетного состояния видно, что те конфигурации, в которых оба электрона находятся по одну сторону от ядра, преобладают, тогда как по контурной диаграмме для триплетного состояния видно, что преобладают конфигурации, имеющие электроны по разные стороны от ядра. В действительности, электроны с одинаковым спином будут иметь максимум вероятности нахождения по разные стороны от ядра на прямой линии, проходящей через ядро т.е. под углом в 180 по отношению друг к другу. Как нетрудно заметить, тот же самый результат был получен ранее при гибридизации атомных s - и р-орбиталей с образованием двух эквивалентных гибридных sp - орбиталей. Единственное отличие здесь в том, что в данном случае рассматривались атомные конфигурации Is p1, а не nslnpl, которые необходимы для образования эквивалентных гибридных орбиталей. Однако это было сделано только для простоты изложения. Угловая корреляция, которая будет рассмотрена далее, не зависит от того, имеют или не имеют s - и р-орбитали одно и то же главное квантовое число. [14]
Страницы: 1 2 3 4 5