Контурная диаграмма
Cтраница 4
 |
Первые два состояния иона Н2. Потенциальные кривые основного и отталкивательного состояний ( а и схема энергетических уровней Hj без учета интеграла перекрывания ( б. [46] |
В нижней части рис. 22, а и б приведены условные контурные диаграммы электронной плотности, напоминающие топографические карты. [47]
Используя волновые функции, полученные в предыдущей задаче, постройте контурную диаграмму электронной плотности для основного состояния нафталина. [48]
 |
Распределение электронной плотности в LiH ( в электронах на кубический ангстрем. [49] |
Для того чтобы получить более полную картину, нам снова понадобится контурная диаграмма, на которой каждая кривая означает линию постоянной вероятности распределения. Так же как на географической карте, здесь можно увидеть области, вероятность пребывания электрона в которых высока, и те области, где эта вероятность мала. На рис. 3.16, а приведена такая карта для LiH; она построена по данным, полученным в последнее время. Еще больше информации можно получить из рис. 3.16, б, на котором представлена разность распределений: из полного электронного распределения ( рис. 3.16, а) вычли некоторое приближение к вероятности идеального обобществления. Эта контурная карта показывает, где в молекуле LiH вероятность распределения выше ( сплошные линии) и где она ниже ( пунктирные линии), чем вероятность, полученная при наложении распределений атома Н и атома Li. На рис. 3.16, б ясно видно, что электроны сдвигаются к атому Н, отходя от более симметричного распределения идеального обобществления электронов. [50]
На рис. 11.6, г разность электронных плотностей передана в виде контурной диаграммы. Здесь линии соединяют точки с равными значениями Ар. Сплошные линии соответствуют положительным значениям Ар: они охватывают область сгущения электронного облака. Штриховые линии отвечают отрицательным значениям Ар: они показывают, где электронная плотность в молекуле меньше, чем в несвязанных атомах. [51]
 |
Изображение 2рг - орбитали. [52] |
Если требуется показать на рисунке точное значение волновой функции, то пользуются контурными диаграммами, где линии соединяют точки, для которых г ( или if2) имеет определенное значение. На рис. 1.8 показаны различные изображения 2р2 - орбитали атома водорода. Форма орбиталей важна для понимания особенностей химической связи, и в дальнейшем мы неоднократно будем пользоваться подобными изображениями орбиталей. На схемах часто рисуют орбитали стилизованно, несколько искажая их форму и пропорции. [53]
 |
Изображение 2р2 - орбитали. [54] |
Если требуется показать на рисунке точное значение волновой функции, то пользуются контурными диаграммами, где линии соединяют точки, для которых i j ( или ф2) имеет определенное значение. На рис. 1.8 показаны различные изображения 2рг - орбитали атома водорода. Несмотря на то, что представленные здесь-фигуры имеют различную форму, они обладают одинаковой симметрией, характерной для рг-орбитали. Форма орбиталей важна для понимания особенностей химической связи, и в дальнейшем мы неоднократно будем пользоваться подобными изображениям орбиталей. На схемах часто рисуют орбитали етилизован-но, несколько искажая их форму и пропорции. [55]
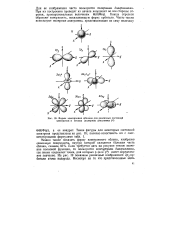 |
Формы электронных облаков для различных состояний электронов в атомах ( полярные диаграммы ф2. [56] |
Если требуется дать на рисунке точное значение волновой функции, то пользуются контурными диаграммами, где линии соединяют точки, для которых ф ( или фа) имеет определенное значение. На рис. 19 показаны различные изображения 2pz - op - битали атома водорода. [57]
К Н - 12 - К1 Н - I, на рис. а показана контурная диаграмма эксперим. [58]
На графике набора потенциальных кривых получаются резко отличные друг от друга линии; каждой потенциальной кривой соответствует контурная диаграмма распределения зарядовых плотностей, имеющая вид сплошного пространственного облака. Чтобы увидеть, как изменяется распределение зарядовой плотности р при образовании молекулы ( в основном состоянии) из распределений в свободных невозбужденных атомах, следует рассмотреть разностную диаграмму распределения Ар, характеризующую отличие основного состояния молекулы О 2 от простого геометрического наложения друг на друга диаграмм свободных атомов. [59]
Принимая во внимание малый размер перетеканий электронной плотности при образовании молекулы, становится ясным, что внешний электрон лития и на контурных диаграммах электронных плотностей молекулярных орбиталей в значительной мере переходит в сферу, окружающую ядро фтора, и связывается с ним большой силой, получающей выражение в энергии сродства электрона к нейтральному атому фтора. При этом для сближения и взаимного проникновения облаков F и Li никакого заметного радиального сдвига для 2р Li-электрона не требуется. Кроме энергии возбуждения 2s - 2р работа не затрачивается на отрывание внешнего электрона от атома лития. [60]
Страницы: 1 2 3 4 5