Активная аминокислота
Cтраница 1
Ферментативный синтез активной аминокислоты из L-метио-нина и аденозин-5 - трифосфата сопровождается выделением в сте-хиометрическом количестве всего фосфора, содержащегося в адено-зин-5 - трифосфате, в виде неорганического фосфата и образованием свободного от фосфора продукта, обладающего ультрафиолетовым спектром поглощения, характерным для производных аденозина. При действии на активный метионин азотистой кислоты происходит дезаминирование ( с образованием производного гипоксан-тина), а при кислотном гидролизе образуется аденин, гомосерин и метилтиорибоза. Гидролиз при рН 6 приводит к гомосерину и 5 -дезокси - 5 -метилтиоаденозину. [1]
В полимерный носитель вводят остатки оптически активной аминокислоты. Через колонку, заполненную таким адсорбентом, пропускается раствор солей меди или другого металла-комплексообразова-теля; при этом металл образует комплекс с закрепленной на носителе аминокислотой. [2]
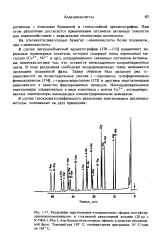
Полученные диастереомеры LIXa и LIX6 дадут два пика на хроматограммах, если исходная оптически активная аминокислота не обладала полной оптической чистотой. [3]
В случае, когда аминоакриловая кислота является частью диоксопиперазинового кольца, содержащего в качестве другой компоненты оптически активную аминокислоту, оптически неактивный гетерогенный катализатор способен к асимметрическому гидрированию с высокой стереоспецифичностью. [4]
В молекуле аланина а-углеродный атом ( он помечен звездочкой) является асимметрическим, и аланин представляет простейшую оптически активную аминокислоту, существующую в виде двух зеркальных изомеров ( стр. [5]
Проблема разделения рацематов аминокислот в промышленном масштабе возникла сравнительно недавно в связи с возросшими потребностями народного хозяйства в оптически активных аминокислотах, играющих важную роль в человеческой жизни. [6]
Другой вариант реализации лигандообменного метода заключается не в ковалентном связывании аминокислоты с сорбентом, а в динамическом модифицировании неполярного сорбента гидрофобным производным оптически активной аминокислоты. Далее на нем фиксируется металл-комплексообразо-ватель, и процесс протекает так же, как в первом случае. [7]
В случае лигандообменной хроматографии [170-173] применяют хи-ральные полимерные носители, которые содержат ионы переходных металлов ( Cu2, Ni2 и др.), координационно связанные оптически активными аминокислотами так, что остаются ненасыщенные координационные связи. В ходе разделения свободные координационные связи занимаются лигандами подвижной фазы. Таким образом был разделен ряд DL-аминокислот на полистирольных смолах с L-пролином, сульфированным фенилаланином [174], L-гидроксипролином [175] и другими энантиомерами аминокислот в качестве фиксированных лигандов. [9]
Субстратом, как правило, служил ацетоуксусный эфир, хотя в ряде случаев использовали и другие соединения, в частности соединения, гидрирование которых приводило к оптически активным аминокислотам. [10]
Недостатком этого метода, так же как и многих других, являлась трудность получения оптически однородных продуктов. В результате реакции оптически активной аминокислоты или пептида с рацемической смесью га-лоидангидридов образуется смесь диастереоизомеров. Снизить выход одного из стереоизомеров можно подбором таких условий, при которых разница скоростей образования диастереоизомеров довольно значительна. Это редкий случай, и поэтому требуется проведать разделение смеси диастереоизомеров дробной кристаллизацией, которую и применял Фишер. Однако, это настолько трудоемкая операция, что он вынужден был направить свое внимание на синтез галоидо-ангидридов оптически активных а-галоидокислот. [11]
Ценный вклад в область стереохимии внесли Фишер и сотрудники [263, 311], получив изомерные дикетопиперазины из дипептидов оптически активных аминокислот. Если дипептид, состоящий из двух структурных единиц одной и той же активной аминокислоты, циклизуется в мягких условиях, то образующийся при этом дикетопиперазин представляет собой одну из активных модификаций t uc - формы. [12]
Индивидуальные диа-стереомеры комплексов Pt ( II) и Pd ( II) с оптически активными аминокислотами могут оказаться биологически активными веществами и составить основу лекарственных препаратов, например, противоопухолевых. [13]
Лишь спустя 34 года Шульце и Босхард [449, 450] показали, что оптически неактивные аминокислоты представляют собой смеси равных количеств право - и левовращающих форм. Если ввести такую оптически неактивную аминокислоту в состав питательной среды для выращивания плесени, то по окончании роста микроорганизма из среды можно выделить оптически активную аминокислоту. [14]
Босхард [394, 396] окончательно установили, что при кислотном гидролизе белка образуются оптичеши активные аминокислоты, которые, обрабатывая баритом, можно перевести в оптически неактивную форму, прячем практически не отличающуюся от оптически неактивной формы аминокислот, образующихся при щелочном гидролизе. При введении такой оптически неактивной аминокислоты в питательную среду плесневого гриба ( Penicillium glaucum) no окончании роста последнего из среды можно было выделить оптически активную аминокислоту. При введении в среду рацематов глютаминовой кислоты и лейцина оптическое вращение аминокислот, выделенных в конце опыта, было примерно равно по величине, но противоположно по знаку оптическому вращению препаратов лейцина и глютаминовой кислоты, выделенных из кислотного гидролизата. Этим было показано, что неактивные аминокислоты являются смесью равных количеств право-и левовращающих форм. [15]
Страницы: 1 2