Абсорбция - окись - углерод
Cтраница 2
 |
К расчету числа тарелок ( схема потоков в колонне. [16] |
В промывной колонне происходит абсорбция окиси углерода жидким азотом. При хорошей промывке азото-водородной смеси в ней остается не более 1 CMS / MS СО. [17]
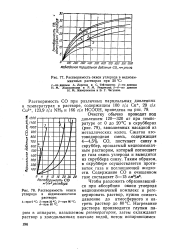 |
Растворимость окиси углерода в медноам.| Растворимость окиси углерода в медноаммиачном. [18] |
Чтобы разложить образовавшийся при абсорбции окиси углерода медноаммиачный комплекс и регенерировать раствор, нужно снизить давление до атмосферного и нагреть раствор до 80 С. [19]
 |
Влияние температуры t газа и азота на расход азота для промывки. [20] |
Расход жидкого азота на абсорбцию окиси углерода при прочих равных условиях зависит не только от концентрации СО в конвертированном газе, но в значительной мере и от содержания в исходной смеси азота и метана. Чем меньше в конвертированном газе метана и азота, тем меньше расход жидкого азота, так как в процессе абсорбции окиси углерода водород насыщается азотом и, следовательно, температура процесса понижается за счет частичного испарения жидкого азота. [21]
Теряет свое значение также способ абсорбции окиси углерода во - 1ой под давлением. Ввиду низкой поглотительной способности воды этот пособ связан с перекачиванием больших масс воды, требует апдарвту - Ы, рассчитанной на повышенное давление, и значительного расхода лекгроэнергии. Получаемая при этом двуокись углерода недостаточно исга. [22]
В первом случае процесс основан на абсорбции окиси углерода водным раствором медноаммиачной соли под давлением 100 - 300 ат при 5 - 20 С. При снижении давления и нагревании до 75 - 80 С комплексное медноаммиачное соединение с СО разрушается с выделением окиси углерода. Раствор охлаждается и возвращается в цикл. [23]
В ГИАПе проводятся опыты по использованию плоско-параллельной насадки для процесса абсорбции окиси углерода медноаммиачным раствором. Как и для случая конденсации водяного пара, применение плоско-параллельной насадки весьма перспективно и ведет к уменьшению габаритов аппарата. Допустимы высокие нагрузки по газу, поскольку это лимитирует сопротивление в газовой фазе. Скорость хемосорбции велика, а сопротивление диффузии в жидкой фазе мало, поэтому малое количество удерживаемой жидкости в данном случае практически не должно оказывать влияния на скорость процесса. [24]
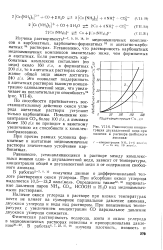 |
Равновесная концентрация двухвалентной меди при наличии в растворе свободного аммиака. [25] |
В работах5 7 - 9 10 получены данные о дифференциальной теплоте растворения окиси углерода. При абсорбции окиси углерода выделяется 10 5 - 13 2 ккал / моль. Определены также32 33 парциальные давления паров NH3, СО2, НСООН и Н О над медноаммиач-ными растворами. [26]
Это условие особенно важно, поскольку в смеси присутствуют непредельные углеводороды. В процессе абсорбции окиси углерода жидким азотом при повышенном давлении и низких температурах ( эти условия способствуют окислению N0 в N02 и в N203) могут образовываться взрывоопасные комплексные соединения сложного состава. [27]
Расход жидкого азота на абсорбцию окиси углерода при прочих равных условиях зависит не только от концентрации СО в конвертированном газе, но в значительной мере и от содержания в исходной смеси азота и метана. Чем меньше в конвертированном газе метана и азота, тем меньше расход жидкого азота, так как в процессе абсорбции окиси углерода водород насыщается азотом и, следовательно, температура процесса понижается за счет частичного испарения жидкого азота. [28]
Для удаления окиси углерода из технического водорода применяются как химические, так и физические методы. К химическим методам очистки водорода от СО относятся процессы, связанные с каталитическим окислением или восстановлением этого соединения, а также процессы, предусматривающие абсорбцию окиси углерода при помощи растворов химических реагентов. Следует отметить, что в ряде случаев - при значительном содержании СО в исходном газе - процесс удаления окиси углерода из газа совмещается с использованием этого соединения для получения другого целевого продукта / Указанное имеет место, например, при каталитической конверсии СО с водяным паром ( с целью получения дополнительных количеств водорода) или при применении СО для синтеза метанола. [29]
Некоторые исследователи полагают, что в реакции абсорбции СО участвует только активный аммиак. Согласно их представлениям, аммиак, связанный в комплексные соединения с двухвалентной медью, и аммиак, образующий с СО2 карбонат аммония, пассивен в реакции абсорбции окиси углерода. [30]
Страницы: 1 2 3