Отдельные аминокислота
Cтраница 1
 |
Хроматограмма кислот. [1] |
Отдельные аминокислоты в разной степени удерживаются бумагой и отстают от фронта растворителя. [2]
Производные отдельных аминокислот при облучении инсулина еще не установлены; это остается важной задачей. [3]
Поскольку отдельные аминокислоты в данном разделе многократно упоминаются в связи с различными способами расщепления, формулы их сведены в табл. 23, чтобы избежать повторения. [4]
Для отдельных аминокислот пригодны также приведенные ниже реакции. [5]
Выделение отдельных аминокислот из белкового гидролизата не сопровождается никакими затруднениями в тех случаях, когда они содержатся в достаточно высоких концентрациях и заметно отличаются друг от друга по свойствам. [6]
 |
Камеры для хроматографии нисходящей ( о и восходящей ( б. [7] |
Положение отдельных аминокислот на фильтровальной бумаге обнаруживают при помощи цветной реакции с нингидрином. [8]
Расположение пятен отдельных аминокислот на общей хромато-грамме устанавливают по контрольным хроматограммам, полученным для каждой аминокислоты в отдельности. [10]
Возможность включения отдельных аминокислот в белки была впервые показана после того, как в биохимических исследованиях стали применять аминокислоты, меченные радиоактивным углеродом, тяжелым азотом или радиоактивной серой. Механизм этого процесса тесно связан с биосинтезом белка заново. Аминокислоты перед включением в белок должны быть активированы. Активация аминокислот осуществляется под действием АТФ с образованием аденилатов аминокислот. Включение аминокислот в белки тесно связано с нуклеиновыми кислотами. [11]
Для определения отдельных аминокислот разработан ряд специфических методов. [12]
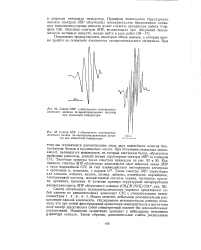
При облучении отдельных аминокислот, являющихся мономерами, из которых построены белки, образуются свободные радикалы, дающие весьма характерные спектры ЭПР со сложной СТС. Такие спектры ЭПР характерны для глицина, аланина, валина, лизина, лейцина, изолейцина, норлейцина, глютаминовой кислоты, аспарагиновой кислоты, серина, гистидина, проли-на, аргинина, треонина. [14]
Переход от отдельных аминокислот или простой их комбинации из нескольких единиц к сочетанию сотен или многих тысяч аминокислотных остатков дает качественный скачок к новому уровню организации материи. Такой более высокий уровень организации называют макроструктурой белковой молекулы. Сюда относятся такие свойства ее, как глобулярная форма, реакции на изменение окружающей среды, а также некоторые уже биологические закономерности. Она становится участником процессов обмена веществ и может выступать, например, в качестве фермента или приобретать свойства иммунной активности. [15]
Страницы: 1 2 3 4