Аурат
Cтраница 3
Для получения монодиеперсных золей золота этим способом в раствор перед восстановлением вводят зародышевый золь золота ( т.е. очень высокодисперсный), приготовленный отдельно путем восстановления хлорида золота фосфором. Золото, выделяющееся при восстановлении аурата калия в присутствии зародышевого золя, равномерно распределяется на зародышах, что и обеспечивает монодисперсность конечного золя. Все выделяющееся золото-отлагается на зародышах, и в полученном золе образуется столько частиц, сколько было введено зародышей. Размер частиц такого-золя, очевидно, тем больше, чем меньше зародышей было введено-в раствор перед восстановлением. Зародышевый способ получения монодисперсных коллоидных систем с частицами желаемого размера широко используется при проведении ряда исследований в коллоидной химии. [31]
Для получения монодиоперсных золей золота этим способом в раствор перед восстановлением вводят зародышевый золь золота ( т.е. очень высоко дисперсный), приготовленный отдельно путем восстановления хлорида золота фосфором. Золото, выделяющееся при восстановлении аурата калия в присутствии зародышевого золя, равномерно распределяется на зародышах, что и обеспечивает монодисперсность конечного золя. Все выделяющееся золото-отлагается на зародышах, и в полученном золе образуется столько частиц, сколько было введено зародышей. Размер частиц такого золя, очевидно, тем больше, чем меньше зародышей было введено-в раствор перед восстановлением. [32]
Все соединения разрушаются при температуре выше 40 - 50 С вследствие восстановления золота и чувствительны к свету. Аураты второй и третьей групп ( за исключением ауратов Си, Cd и Ва) не образуют кристаллических осадков. [33]
Соединение Na [ Au02 ] - H20 представляет собой зеленые кристаллы, которые растворяются в воде и плохо растворимы в спирте. Двуокись серы и щавелевая кислота восстанавливают при нагревании в водных растворах аураты и основные аураты щелочных металлов до металлического золота. [34]
Соединение Na [ Au02 ] - H20 представляет собой зеленые кристаллы, которые растворяются в воде и плохо растворимы в спирте. Двуокись серы и щавелевая кислота восстанавливают при нагревании в водных растворах аураты и основные аураты щелочных металлов до металлического золота. [35]
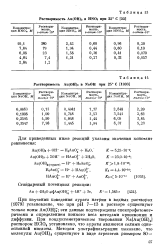 |
Растворимость Au ( OH3 в HNOs при 25 С.| Растворимость Аи ( ОН з в NaOH при 25 С. [36] |
При изучении поведения аурата натрия в водных растворах [1079] установлено, что при рН 7 - 13 в растворе существуют только ионы Au ( OH) I; эти данные подтверждены спектрофотомет-рически и определением ионного веса методами криоскопии и диффузии. При кондуктометрическом титровании Na [ Au ( OH) 4 ] раствором НСЮ4 установлено, что аураты являются солями одноосновной кислоты. [37]
Оксид трехвалентного золота ( Аи2О3) ( ангидрид золота) - коричневый порошок; соответствующая кислота - гидроксид золота или золотая кислота ( Аи ( ОН) 3), черный продукт, разлагающийся на свету, из которого получают щелочные аураты. [38]
При действии хлора на порошок золота при 200 образуется АиС13 - х лорное золото коричнево-красного цвета. Гидроокись золота является амфотерным соединением, преимущественно кислотного характера, и называется также золотой кислотой. Соли этой, кислоты называются ауратами. [39]
Соединения золота с кислородом неустойчивы. Это соединение быстро разлагает-ся. Гидрат окиси золота образуется при гидролизе некоторых солей золота ( III) или путем разложения ауратов кислотой. [40]
Соединения золота с кислородом неустойчивы. Это соединение быстро разлагается. Гидрат окиси золота образуется при гидролизе некоторых солей золота ( III) или путем разложения ауратов кислотой. [41]
Цианид не разрушается разбавленными кислотами и сероводородом, и очень мало или, вернее, почти не растворим в воде. Однако он достаточно легко растворяется в цианидах щелочных металлов с образованием соответствующих комплексных солей типа Me [ Au ( CN) 2 ] дициано - ( 1) ауратов. [42]
При добавлении к АиС13 соляной кислоты цвет раствора меняется на лимонно-желтый. Этот раствор содержит соединение Н [ АиС14 ], обладающее свойствами кислоты. Ее называют золотохлористоводородной или тетра-хлоро - ( 1П) золотой кислотой. В лабораторной практике и в технике под названием хлорное золото разумеют тетрахлоро - ( Ш) аурат натрия Na [ AuCl4 ] 2Н2О, хорошо растворимый в воде и эфире, его часто называют золотой солью; и аналогичную соль калия - KtAuClJ 2Н2О - кристаллы желтого цвета, растворимые в воде, но не растворимые в эфире. [43]
Страницы: 1 2 3