Ацеталь - ацетальдегид
Cтраница 1
Ацетали ацетальдегида [44, 728, 794, 800-805], пропионового альдегида [44, 794, 798, 806, 807], масляного альдегида [41, 807] и изомасляного альдегида [44, 807] гладко реагируют с разнообразными виниловыми эфирами. При этом всегда образуется смесь теломеров. [1]
 |
Результаты определения остаточного сезамекса на стекле. [2] |
Ацетали ацетальдегида ведут себя подобным же образом: кислота гидролизует CH3CH ( OR) 2 в СН3СН ( ОН) 2, являющийся гидратированной формой ацетальдегида. [3]
Получение ацеталей ацетальдегида нзаимодействием ацетилена со спиртами в присутствии кислот известно уже давно. Эти ацетали образуются также при присоединении дополнительной молекулы спирта к простому виниловому эфиру. [4]
Удобным диенофилом оказался циклический ацеталь ацетальдегида с ыс-бутен-2 - диолом-1 4 ( CXLIV), который получают ацетализацией цис-бутен-2 - диола-1 4 ( CXLIII) ацетальдегидом в присутствии каталитических количеств соляной кислоты. [5]
Аналогичная реакция проходит между ацеталями ацетальдегида и ацетона с ацетамидом в уксусной кислоте в присутствии концентрированной серной кислоты в условиях гидрирования с 10 % - ным палладием на угле. [6]
В этом случае также получается соответствующий ацеталь ацетальдегида. Самым активным катализатором этого процесса является смесь окиси ртути и фтористого бора; менее активной является пара: сульфат ртути и концентрированная серная кислота. Здесь также в виде промежуточного продукта присоединения спирта к винилацетату образуется вещество, которое тотчас же переходит в ацеталь и фир уксусной кислоты. [7]
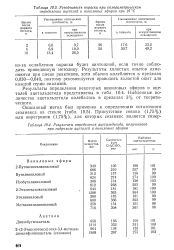 |
Устойчивость окраски при колориметрическом определении ацеталей и виниловых эфиров при 25 С.| Результаты определения ацетальдегида, полученного при гидролизе ацеталей и виниловых эфиров. [8] |
Результаты определения некоторых виниловых эфиров и ацеталей ацетальдегида представлены в табл. 10.4. Найденные количества ацетальдегида колебались в пределах 3 % от теоретического. [9]
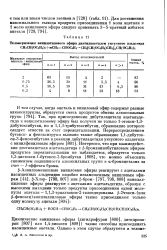 |
Телоиеризация винилэтилового эфира диэтилацеталем уксусного альдегида. [10] |
Хлор - [798, 807] или р-бром - [797, 798, 808] винилал-киловые эфиры реагируют с ацеталями ацетальдегида, образуя с высокими выходами только продукты присоединения одной молекулы ацеталя - 1 1 3-триалкокси - 2-галоидпропаны. [11]
По сообщению фирмы Du Pont5, при действии ацетилена на моно-эфиры полигликолей в присутствии солей ртути кремнефтористоводород-ной кислоты образуются ацетали ацетальдегида. С при 14 мм рт. ст.), из вторичного ацетата целлюлозы образуются очень прозрачные, очень мягкие эластично пленки, свойства которых не ухудшаются даже после 3 месяцев хранения. [12]
Варьируя заместители R и RI в виниловом эфире и спирте, можно приготовить разнообразные, часто труднодоступные иными путями симметричные и несимметричные ацетали ацетальдегида. [13]
При изучении механизма этой реакции было высказано предположение, что в случае взаимодействия меркур-бас-ацеталъдегида с кетеном в спирте реакция идет через промежуточное образование ацеталя меркурированного ацетальдегида. С целью дальнейшего расширения области найденной реакции и доказательства предложенного механизма изучено действие диме-ра кетена на а-меркурировашше карбонильные соединения. [14]
По данным Хорнера [85], в отличие от хлоруглеводородов, содержащих С13 - группу, претерпевающих при гидрировании над скелетным никелем в присутствии основания димеризацию с образованием группировки СС12СС12 - ( см. выше), такие соединения, как а р р р-тетрахлорэтиловый эфир, диэтилацеталь хлораля, трихлоруксусная кислота в тех же условиях гладко восстанавливаются в диэтиловый эфир, ацеталь ацетальдегида и уксусную кислоту соответственно. [15]
Страницы: 1 2