Ацетил-холинэстераза
Cтраница 1
Активность ацетил-холинэстеразы в мозге крыс в условиях моделирования алкогольной эмбриопатии / / Жури, невропатологии и психиатрии. [1]
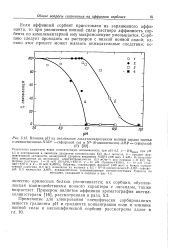 |
Влияние рН на связывание лактатдегидрогеназы мышцы сердца свиньи е-аминогексаноил - МАВ - сефарозой ( а и № - ( 6-аминогексил - АМР - сефарозой. [2] |
Примером является аффинная хроматография ацетил-холинэстеразы [16], рассмотренная в разд. [3]
 |
Схема передачи нервных импульсов. [4] |
Разрушение ацетилхолина осуществляется ферментом ацетил-холинэстеразой. [5]
 |
Местные анестетики. [6] |
Инактивация медиатора путем гидролиза тормозится ингибиторами ацетил-холинэстеразы. Вещества, действующие постсинаптически, можно разделить на две группы. Соединения одной группы, например ре-цепторные антагонисты типа кураре и сс-нейротоксины из змеиных ядов кобры и крайта, блокируют связывание медиатора и рецептора. Другая группа соединений, по-видимому, имеет отношение к событиям, протекающим вслед за образованием медиатор-рецепторного комплекса. [7]
Различают 2 типа холинэстеразы: истинную, содержащуюся преимущественно в тканях нервной системы-в скелетной мускулатуре, а также в эритроцитах, и ложную, содержащуюся главным образом в плазме крови, печени и некоторых других органах. Собственно ацетил-холинэстеразой является истинная, или специфическая; холинэстераза, так как только она гидролизует названный медиатор. И именно ее в дальнейшем мы будем обозначать термином холинэстераза. Поскольку фермент и медиатор являются необходимыми химическими компонентами передачи нервных импульсов в синапсах - контактах между двумя нейронами или окончаниями нейрона и рецепторной клеткой, следует более подробно остановиться на их биохимической. [8]
Как видно из приведенных рисунков, величина оптимума рН не столь типична для различения холинэстераз и ацетилхолинэстераз, как это иногда отмечалось в литературе. Во-первых, ацетил-холинэстеразы разного происхождения различаются в этом отношении между собой. Во-вторых, оптимум рН одного и того же фермента может зависеть от структуры субстрата. [10]
О нарушении функционального состояния печени свидетельствует снижение активности ацетил-холинэстеразы и повышение активности аспарагиновой транс-аминазы. [11]
К важнейшим контактным инсектицидам относятся и многочисленные органические производные фосфора: производные фосфорной, тио - и дитиофосфорной, фосфоновой кислот. Все соединения этого класса являются фосфорилирующи-ми агентами и фосфорилируют ферменты вредителя ( ацетил-холинэстеразу), нарушая его жизненные функции. Их общий недостаток - токсичность для теплокровных, хотя для отдельных представителей она и не очень высока. Замена в группировке фосфорной кислоты атомов кислорода на серу, как правило, несколько снижает токсичность, не уменьшая инсектицидную активность. Все многочисленные производные этого класса довольно быстро дезактивируются в природе вследствие гидролитических процессов и процессов окисления. Процессы метаболизма также идут довольно быстро. [12]
В ложной холинэстеразе на каждый эстеразный центр приходится один анионный центр, а в ацетилхолинэстеразе - два. С другой стороны, Адаме и Уиттакер [1 ], исходя из различий во взаимодействии холина с этими двумя ферментами, показали, что ацетил-холинэстераза должна иметь на один центр больше, чем сывороточная холинэстераза. [13]
В табл. 13 приведены основные данные для ацетилхолинэстеразы эритроцитов и нервной ткани различных животных. Константы Михаэлиса для ацетилхолинэстераз, как видно из данных этой таблицы, как правило, значительно ниже константы холинэстераз, что свидетельствует о большем сродстве ацетилхолина к ацетил-холинэстеразам. [14]
Вторым направлением развития метода потенциометрического титрования является создание способа поддержания в ходе ферментативной реакции постоянства концентрации субстрата в реакционной среде. Необходимость такого метода диктуется особенностями кинетики реакций, катализируемых ацетилхолинэстеразой и некоторыми другими ферментами, активность которых тормозится уже при сравнительно низких концентрациях субстрата. При изучении кинетики таких реакций во избежание субстратного торможения приходится работать в области концентраций, не достигающих насыщения фермента. С другой стороны, при высокой молекулярной активности фермента ( как, например, в случае ацетил-холинэстеразы) это приводит к быстрому снижению концентрации субстрата и переходу из кинетической области нулевого порядка к мономолекулярной, что затрудняет вычисление начальной скорости реакции. [15]
Страницы: 1 2
