Защищенные аминокислота
Cтраница 1
Защищенные аминокислоты должны получаться легко и желательно с количественным выходом. Защитные группы должны сохранять свои блокирующие свойства для возможно большего числа методов синтеза пептидов. Они не должны вызывать побочных реакций. Они должны легко и селективно удаляться, чтобы не затрагивались другие защитные группы той же самой или другой функциональной группировки. На практике все эти условия одновременно никогда не выполняются, поэтому часто приходится останавливаться на компромиссном решении. Вот почему потребность в новых защитных группах и их подходящих комбинациях остается одной из главных проблем химии пептидов. [1]
 |
Структура дициклогексилкарбодиимида ( ДЦГК и дициклогексил. [2] |
Простое смешивание подходящим образом защищенных аминокислот приводит к образованию соли. Поэтому для того, чтобы прошла конденсация, реагенты нужно активировать. Предварительное превращение карбоксильной группы в ацил-хлорид - весьма эффективная активация, но для этого требуется дополнительная стадия, иногда приводящая к неприемлемо большой степени рацемизации. Более удобно использовать конденсирующие агенты, которые непосредственно добавляются к смеси защищенных аминокислот. Он вначале реагирует с карбоксильной группой, образуя активированное производное, которое затем взаимодействует со свободной аминогруппой, давая защищенный дипептид и дициклогек-силмочевину. [3]
Активация карбокоильной группы - защищенных аминокислот при помощи цианамида во многом близка процессу, происходящему при ДЦГК-методе. [4]
Смешанные ангидриды / - защищенных аминокислот или пептидов с бенаол-сульфокислотой приводят к полной рацемизации. Однако использование - метилморфолина в качеотве основания вместо триэтилаыияа в. [5]
Активированные эфиры нового типа были получены при обработке защищенных аминокислот или пептидов в ацетонитриле или в ниг-рометане этил-5 - ( 3 -сульфофенил) - оксазолом. [6]
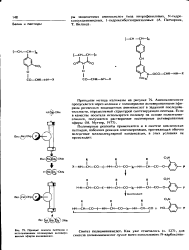 |
Принцип синтеза пептидов с ix. t v. [7] |
Аминокомпонент пропускается через колонки с полимерными активированными эфи-рами различных защищенных аминокислот в заданной последовательности, определяемой структурой синтезируемого пептида. [8]
Активированные эфиры нового типа, были получены при обработке защищенных аминокислот или пептидов в ацетонитриле или в нит-рометане М - этил-5 - ( 3 -сульфофенил) - оксазолом. [9]
В табл. 9 представлены свойства л-нитрофекияовнх эфиров / - защищенных аминокислот, полученных разными методами. [10]
Под этим названием известны пептидные синтезы, включающие отщепление воды от защищенных аминокислот или пептидов и эфиров аминокислот с использованием реагентов, переходящих при этом в гидратную форму. [11]
В табл. 44 приведены физико-химические характеристики оивтези-рованннх пентафторфениловых эфиров / - защищенных аминокислот. [12]
Синтез последних соединений из метиловых, этиловых или бензиновых эфиров / - защищенных аминокислот и пептидов также не предотавляет большого труда. [13]
В табл. I приведены основные методы я реагенты активации карбоксильной группы N - защищенных аминокислот и пептидов. Часть из них хорошо себя зарекомендовала и находит широкое применение в синтезе пептидов, а некоторые предложены недавно, но весьма перспективны. [14]
СУБТИЛИЗИНЫ, ферменты класса гидролаз, катализирующие гидролиз белков и пептидов, а также сложных эфиров и амидов М - защищенных аминокислот. [15]
Страницы: 1 2