Линия - азеотроп
Cтраница 2
Выразим в терминах активности уравнение (2.55) для линии азеотропов, когда пар подчиняется законам идеальных газов. В том случае, когда второй компонент диссоциирован, знаменатель будет стремиться к бесконечности. [16]
Выражения (2.51) и (2.52) представляют собой уравнения линии азеотропов в соответствующих координатах. Эти уравнения соблюдаются во всей области существования азеотропов вплоть до критической точки. [17]
В системе же этанол - этила-цетат ( 2) линия азеотропов идет при низких температурах в области концентрированных растворов ( по-видимому, она доходит до температуры замерзания) и заканчивается на оси чистого этанола, далеко не доходя до критических параметров системы. [18]
Вопрос о том, где на диаграмме должна проходить линия азеотропов и где должна быть критическая точка азеотропа, в общем случае определяется соотношением (2.51) или (2.52) и пригодным для этой области параметров уравнением состояния системы. [19]
С повышением давления область гетерогенного равновесия, через которую проходит линия азеотропов с максимальной температурой кипения, будет сужаться. [20]
Иногда, напротив, они возникают у оси чистого компонента, а линия азеотропов проходит затем в области концентрированных растворов вплото до критической кривой. В некоторых же системах вся линия азеотропов лежит где-то в средней части концентрационного интервала. О системах двух последних типов говорят, что они обладают открытой областью азео-тропизма. [21]
Используется принцип соответственных состояний [15], методы статистической физики [16], а также эмпирические методы ( например, определение параметров азеотропной смеси по линии азеотропов для данного азеотропного ряда [1]) и эмпирические соотношения. [22]
Из литературы [6] было известно, что в системе этилен - двуокись углерода азеотропизм обнаруживается только начиная примерно с 4 бар. Линия азеотропов начинается где-то от оси чистого этилена. [23]
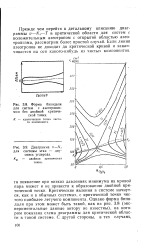 |
Форма бинодали для систем с азеотропиз-мом без двойной критической точки.| Диаграмма w - JV-для системы этан - двуокись углерода. [24] |
Прежде чем перейти к детальному описанию диаграммы v - Ni - Т в критической области для систем с положительным азеотропом с открытой областью азео-тропизма, рассмотрим более простой случай. Если линия азеотропов не доходит до критической кривой и заканчивается на оси какого-нибудь из чистых компонентов. [25]
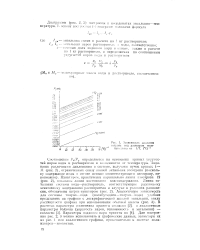 |
Зависимость давления. [26] |
Соотношение PB / PV определяется на основании кривых упругос-тей паров воды и растворителя в зависимости от температуры. Пунктиром, практически параллельно линии азеотропа 12 ( рис. 2), показаны линии постоянного влагосодержания. Для построения рис. 2, 3 можно использовать и графические данные, заимствуя их из рис. 1 или аналогичного графика, применительно к системе поли-изоп реи-из () п е 1i тан. [27]
Иногда, напротив, они возникают у оси чистого компонента, а линия азеотропов проходит затем в области концентрированных растворов вплото до критической кривой. В некоторых же системах вся линия азеотропов лежит где-то в средней части концентрационного интервала. О системах двух последних типов говорят, что они обладают открытой областью азео-тропизма. [28]
Среди бинарных растворов отрицат. Эта зависимость на фазовой диаграмме образует линию азеотропов, которая может проходить через всю область существования равновесия жидкость-пар, вплоть до критич. Возможно состояние, когда азеотропная точка сместится за край фазовой диаграммы и А. [29]
Одной из наиболее изученных при высоких давлениях систем с азеотропизмом является система этан - двуокись углерода. Пунктирная кривая, соединяющая максимумы на изотермах, - линия азеотропов. Из приведенных данных видно, что азеотропные смеси в этой системе, начиная от низких температур, представляют собой концентрированные растворы. Видно также, что составы азеотропов сравнительно мало меняются с температурой, и, следовательно, производные ( dP / dN) a3 и ( dT / dNi) a3 велики. [30]
Страницы: 1 2 3