Эвтектическая диаграмма
Cтраница 1
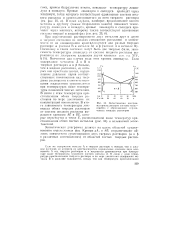 |
Эвтектическая диаграмма кристаллизации системы медь - серебро с образованием ограниченных твердых растворов. [1] |
Эвтектическая диаграмма делится на шесть областей существования определенных фаз. Кривые аА и ЬВ отграничивают область совместного существования двух твердых растворов ( а и р в различных соотношениях) от областей чистых твердых растворов. [2]
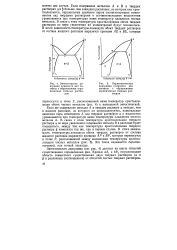 |
Эвтектическая диаграмма плавкости для системы с образованием ограниченных твердых растворов.| Перитектическая диаграмма плавкости для системы с образованием ограниченных твердых растворов. [3] |
Эвтектическая диаграмма ( см. рис. 4) делится на шесть областей существования определенных фаз. Кривые aAi и ЬВг отграничивают область совместного существования двух твердых растворов ( а и ( 3 в различных соотношениях) от областей чистых твердых растворов. [4]
Форма эвтектической диаграммы зависит от разности температур плавления компонентов А и В. Если температуры плавления близки, точка Е лежит примерно посередине диаграммы. [5]
Форма эвтектической диаграммы зависит от разности температур плавления А и В. Если температуры плавления близки, точка Е лежит примерно посередине диаграммы. [6]
Общий тип эвтектической диаграммы, представленный на рис. 6, характеризуется непрерывным увеличением концентрации твердого раствора по мере понижения кривой солидуса от точки А к точке С. Это означает, что с понижением температуры решетка основного металла А может принимать постепенно увеличивающееся количество компонента В до тех пор, пока в равновесии участвует жидкая фаза. Может случиться, однако, что с понижением температуры решетка перестает принимать атомы растворяемого компонента. [7]
 |
Домены в магнитных материалах ( но Киттелю. [8] |
В случае эвтектической диаграммы с твердыми растворами из каких фаз состоит эвтектика. [9]
Общий тип эвтектической диаграммы, представленный на рис. 6, характеризуется непрерывным увеличением концентрации твердого раствора по мере понижения кривой солидуса от точки А к точке С. Это означает, что с понижением температуры решетка основного металла А может принимать постепенно увеличивающееся количество компонента В до тех пор, пока в равновесии участвует жидкая фаза. Может случиться, однако, что с понижением температуры решетка перестает принимать атомы растворяемого компонента. [10]
 |
Дистектическая диаграмма состояния без твердых растворов и с одним химическим соединением. [11] |
На рис. 8 изображена эвтектическая диаграмма состояния системы Ag - Си с ограниченными твердыми растворами. Рассмотрим, например, сплав 15 % Си и 85 % Ag. С дальнейшим понижением температуры до 779 С ( ТЕ) состав жидкой фазы изменяется по линии ФЕ, а состав кристаллов а-фазы - по линии НА. Таким образом, в эвтектической точке Е находятся в нонвариантном равновесии три фазы: жидкая ( 28 5 % Си и 71 5 % Ag) и два твердых раствора - а и Р упомянутого состава. Эвтектический расплав затвердевает без изменения состава при постоянной температуре. [12]
На рис. 8 изображена эвтектическая диаграмма состояния системы Ag-Си с ограниченными твердыми растворами. Поле 1 - область существования одной жидкой фазы, в поле 2 сосуществуют расплав и твердый раствор меди в серебре ( а-фаза), в поле 3 - расплав и твердый раствор серебра в меди ( р-фаза), в поле 4 - однородный твердый раствор а, в поле 5 - однородный твердый раствор р, в поле 6 - механическая смесь кристаллов аир. Рассмотрим, например, сплав 15 % Си и 85 % Ag. С дальнейшим понижением температуры до 779 С ( точка Е) состав жидкой фазы изменяется по линии ФЕ, а состав кристаллов а-фазы - по линии НА. [13]
Сурьма со свинцом дает эвтектическую диаграмму состояния. Эвтектика содержит 12 % сурьмы и 88 % свинца. Обычно такой высокий процент содержания сурьмы не применяют вследствие хрупкости получаемого сплава. В большинстве случаев достаточно иметь в сплаве не более 2 % сурьмы, что обеспечивает содержание донорных примесей порядка 1 4 102 атомов в 1 см3 при температуре плавления около 600 С. [14]
Оказалось, что кривые ликвидуса эвтектических диаграмм плавности описываются, уравнением Шредера в широких концентрационных пределах, вплоть до эвтектики. Применяя уравнение Шредера и используя данные термического анализа таких систем, можно определять молекулярный вес с большой точностью. Применение метода термического анализа систем для определения молекулярного веса позволяет значительно увеличить число веществ, пригодных к использованию в качестве растворителей при крносколическом определении молекулярного веса. [15]
Страницы: 1 2 3 4 5