Замещенный ацетофенон
Cтраница 1
Замещенные ацетофеноны ( см. табл. 5.4.1), которые используются в промышленности в гораздо меньших масштабах ( главным образом в парфюмерии), получают ацилированием по Фриделю - Крафтсу ( см. разд. [1]
Замещенные ацетофеноны ( см. табл. 5.4.1), которые используются в промышленности в гораздо меньших масштабах ( главным образом в парфюмерии), получают ацилированисм по Фрнделю - Крафтсу ( см. разд. [2]
Скорость окисления замещенных ацетофенонов сильно зависит от характера заместителя. [3]
В - замещенных ацетофенонах в среде абсолютного дейте-роэтилового спирта в присутствии этилата натрия происходит обмен водорода в группе СН3 на дейтерий. [4]
Мускус-кетон является динитропроизводным замещенного ацетофенона. [5]
Пространственные препятствия проявляются также в реакциях opro - замещенных ацетофенонов. Карбонильная группа незамещенного ацетофенона располагается целиком в плоскости бензольного кольца IX. Взаимодействующие с карбонильной группой реагенты имеют возможность приблизиться к ней, подходя перпендикулярно к бензольному кольцу. [6]
В классических работах Цукера и Гаммета [95, 96] по изучению замещенных ацетофенонов было показано, что реакции енолизации подчиняются механизму общего катализа. [7]
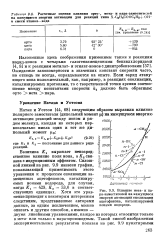
На рис. 6.3 изображен график в координатах: величины рЛГвнЭ замещенных ацетофенонов - величины а для соответствующих заместителей. [8]
Имеется, по-видимому, связь между характером заместителей в ядре замещенных ацетофенонов и величиной изотопного эффекта при образовании их 2 4-динитрофенилгидразонов ( № 37 - 39 табл. 30): заместители, оттягивающие электроны, уменьшают изотопный эффект, а отталкивающие электроны - увеличивают его. [9]
Они рассматривают его на примере каталитической реакции, протекающей в несколько стадий, а именно бромирования замещенных ацетофенонов под влиянием кислот. [10]
В заключение необходимо подчеркнуть, что образование оснований Шиффа из замещенных бензальдегидов и w - бутиламина в области - с-заместителей качественно соответствует образованию циангидринов, а в области ст-заместителей - протонировангоо замещенных ацетофенонов. В первой из упомянутых областей решающей является реакция присоединения, во-второй - реакция отщепления воды. [11]
Итак, можно обобщить вышеизложенное следующим образом: образование оснований Шиффа из замещенных бензальдегидов и к-бутиламнна в области отрицательных а весьма напоминает реакцию образования циангидринов, а в области положительных о - реакцию протонированкя замещенных ацетофенонов. [12]
Однако в тех случаях, когда R представляет собой ароматический, a R, наоборот, алифатический остаток, в результате кислотного гидролиза получается почти исключительно жирноаро-матический кетон: так, например, из бензоилацетона С6Н5 - СО - СН2 - СО - СН3 получается таким образом ацетофенон, а из замещенных бензоилацетонов - замещенные ацетофеноны ( см. стр. [13]
Однако в тех случаях, когда R представляет собой ароматический, а R, наоборот, алифатический остаток, в результате кислотного гидролиза получается почти исключительно жир-ноароматический кетон: так, например, из бензоилацетона СвН5 - СО-СН2 СО - СН3 получается таким образом ацетофенон, а из замещенных бе л зоил ацетоне в - замещенные ацетофеноны ( см. стр. [14]
Страницы: 1 2