Red-форма
Cтраница 1
Red-формы - выражена отчетливо, Ен для систем Сг3 2 и Мп3 2 заметно ниже, чем можно было ожидать. [1]
При внешнесферном механизме Ох - и Red-формы в переходном комплексе взаимодействуют слабо и имеют близкую структуру внутренней координационной сферы. В случаях внутри-сферного механизма в переходном комплексе образуются мостики, облегчающие электронный обмен. Такими мостиками служат частицы, которые являются составной частью внутренних координационных сфер Ох - или Red-форм; ионы Н или ОН - часто способны выполнять эту роль. Внешнесферный механизм, как правило, установлен в тех случаях, когда частицы, составляющие внутреннюю координационную сферу, являются весьма инертными. И наоборот, в случае их высокой лабильности следует ожидать внутрисферный механизм. [2]
 |
Электрохимический диод - интегратор дискретного действия ( а и непрерывного действия ( б. [3] |
Обычно концентрация одной из форм ( например, Red-формы) значительно больше другой п ее изменением можно пренебречь. [4]
 |
Электрохимический диод - интегратор дискретного действия ( а и непрерывного действия ( б. [5] |
Обычно концентрация одной из форм ( например, Red-формы) значительно больше другой и ее изменением можно пренебречь. [6]
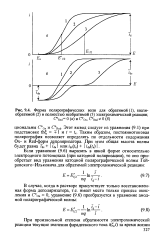 |
Форма полярографических волн для обратимой ( 1, квазиобратимой ( 2 и полностью необратимой ( 3 электрохимической реакции. C Red 0 ( а и С 0х, C Red 0 ( б. [7] |
Таким образом, постояннотоковая полярография позволяет определять по отдельности содержания Ох - и Red-форм деполяризатора. [8]
В двойном знаке верхний знак относится к Ox-форме деполяризатора, а нижний - к Red-форме. [9]
Величина г может быть также найдена по изменению степеней окисления г элемента, входящего в сопряженные Ох и Red-формы реагирующих веществ. [10]
 |
Вид стационарных поляризационных кривых при т ] RT / nF ( a ai 4 6 RTInP ( в для систем со значениями f 1 ( /, 10 - 2 ( 2 и Ю - ( 3 А см-2. СОх CRed 0 1 м. [11] |
При равновесном потенциале i 0, поэтому градиенты концентраций у поверхности электрода отсутствуют и в (1.23) фигурируют объемные концентрации Ох - и Red-форм. [12]
Из приведенных примеров следует, что расчетный метод не только позволяет обойти трудности нахождения У9кв по сравнению с методом потенциометрического титрования, но и дает возможность определять по отдельности концентрации Ох - и Red-форм. При этом иногда не обязательно добавлять окислитель или восстановитель к анализируемому раствору - можно обойтись стандартной добавкой одного из компонентов анализируемой системы. Это очень важное достоинство расчетного метода, оно позволяет по-новому отнестись к традиционным схемам химического анализа. Например -, в массовых анализах на соотношение Fe ( II) и Fe ( III) обычная методика состоит в том, что в одной из проб титруют Fe ( II) бихроматом или Ce ( IV), а в другой пробе Fe III) восстанавливают в редукторе Джонса и аналогичным титрованием определяют суммарное содержание железа. [13]
В [143] отмечается, что с уменьшением Снсю, Ен при заданном отношении Cox / CRed также уменьшается, и это является правилом для систем, у которых Ox-форма несет больший заряд по сравнению с Red-формой. Уменьшение концентрации фонового электролита желательно для повышения точности определения Е, но часто ограничено из-за гидролиза редокс-компонентов системы. [14]
При небольшом конструктивном изменен in - помещении между электродами ( их размеры в этом случае примерно одшпковы) токопроводящей диафрагмы ( рис. 17.8), предотвращающей смешение растворов и ограничивающей их взаимную диффузию, такой диод может выполнять роль интегратора. При прохождении тока через диод в анодном пространстве возрастает концентрация Ox-формы и уменьшается концентрация Red-формы, а в катодном наоборот. [15]
Страницы: 1 2