Ацилирование - ароматическое соединение
Cтраница 2
Таким образом, ацилирование ароматических соединений хлорангидридами жирных кислот осуществляется чрезвычайно региоселективно в иора-положение. Эти данные находятся в хорошем соответствии с предположением о том, что для производных жирных кислот ацилирующим агентом является объемистый комплекс AlkCOCl А1С13, который атакует ароматический субстрат в пространственно незатрудненное пара-положение. Меньшая селективность хлорангидридов ароматических кислот, возможно, объясняется тем, что в реакции принимает участие катион ацилия или его контактная ионная пара. [16]
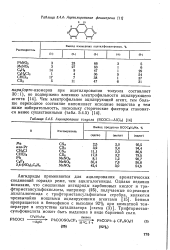 |
Ацетилирование фенантрена.| Ацилирование толуола ( RCOC1 - A1CU. [17] |
Ангидриды применяются для ацилирования ароматических соединений гораздо реже, чем ацилгалогениды. Трифторметан-сульфокислота может быть выделена в виде бариевой соли. [18]
Общим методом получения красителей данной группы является ацилирование соответствующих ароматических соединений бензоилхлоридом в присутствии хлорида алюминия с последующим превращением образовавшихся ароматических кетонов в хиноны путем циклизации с одновременным дегидрированием. [19]
Внимание советских химиков привлекали также электрофильные реакции ацилирования ароматических соединений по Фриделю - Крафт-су действием галогенангидридов карбоновых кислот в присутствии га-логенидов алюминия, приводящие к получению карбонильных соединений. [20]
Фри-дель - Крафтса; - реакции алкили-рования и ацилирования ароматических соединений с помощью ал-килгалогенидов и галоидангидри-дов кислот, соответственно, в присутствии конденсирующего катализатора ( А. [21]
Электрофильность карбонильных реагентов относительно невелика, поэтому реакции ацилирования ароматических соединений проводят в присутствии катализаторов. [22]
Механизм ацетилирования енолацетатов уксусным ангидридом с образованием моноенолацетатов р-дикетонов аналогичен механизму ацилирования ароматических соединений по Фри-делю - Крафтсу. [23]
Применение Bids в качестве эффективного катализатора реакций ацилирования ароматических эфиров известно, но нет строгих доказательств его эффективности для ацилирования неактивированных ароматических соединений. Однако потенциал использования широкого ряда солей Bi ( III) в качестве катализаторов, особенно оксида, оксихлорида и карбоксилатов, представляется важным. Возможности, имеющиеся в этой области, изложены в обзоре [281], содержащем более 50 ссылок. [24]
Эти результаты ясно показывают, что ионы ацилония RCO могут существовать в серной кислоте и в нитрометане и что они значительно более активные ацилирующие агенты, чем протонированная кислота RC02H2 Эти сведения также дают основание предполагать, что в некоторых хлоридах кислот, как 2 4 6-трибром - и 2 4 6-триметилбензоилхлорид, происходит ионизация в соответствующие ацилоний-ионы и ацилирование ароматических соединений идет, по-видимому, через эти ионные промежуточные соединения. [25]
С в присутствии ВС13, образующего, как и при алкилировании ( см. разд. Об ацилировании ароматических соединений Л У-дизаме-щенными карбаксамидами, применяемом главным / образом для получения альдегидов, см. разд. [26]
Ход реакции сложных эфиров с ароматическими соединениями в присутствии хлористого алюминия изменяется в зависимости от природы взятого в реакцию эфира и от условий реакции. Конденсация протекает с предварительным расщеплением эфира и может быть направлена исключительно в сторону алкилирования или ацилирования ароматического соединения. Имеются сведения и об одновременном алкилировании и ацилировании. Прежние исследователи получали обычно смеси алкилиро-ванных и ацилированных продуктов реакции, в позднейших же работах были выяснены оптимальные условия для получения либо кетонов, либо алкшшроиз водных. Каштанов [22] нашел, что при реакции сложных эфиров с бензолом и хлористым алюминием образуется смесь алкилированных и ацилированных продуктов. [27]
Первые работы по алкилированию ароматических углеводу родов относятся к концу XIX в. Крафт ( 1877 г.), а затем Г. Г. Густавсон ( в России) разработали метод ал кгогарования и ацилирования ароматических соединений coof ветственно алкил - и ацилгалогенидами в присутствии хлорид алюминия. [28]
Ацилирование ароматических и гетероциклических соединений, как известно, обычно приводит к монокетонам независимо от соотношения реагентов. Это объясняется дезактивирующим эффектом ацильной группы, который еще более усиливается вследствие образования комплекса с кислотой Льюиса, используемой в качестве конденсирующего агента. Кроме того, комплексы алкиларилкето-нов с льюисовскими кислотами в ряде случаев плохо растворимы в обычных растворителях и выводятся из сферы реакции. По этим причинам образование дикетонов при ацилировании ароматических соединений или их моноацилзамещенных наблюдается лишь в некоторых особых случаях. [29]
Страницы: 1 2