Логарифм - коэффициент - активность
Cтраница 1
Логарифмы коэффициентов активности обычно можно выразить через мольную долю Хг полиномами ( см. гл. Поэтому, система уравнений (8.37) может включать либо логарифмы неизвестных Х % и Х %, либо их разложения в ряд. За исключением нескольких простых случаев, аналогичных рассмотренным в 8.2 и 8.3, найти аналитическое выражение Х % и Х как функцию Т невозможно, и следует искать численные решения. Это делают с помощью компьютера. [1]
Логарифм коэффициента активности воды в растворах КС1 при больших концентрациях отрицателен. Поэтому следует принять для растворов К. [2]
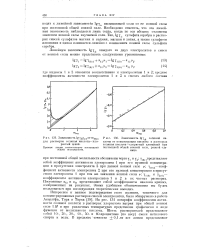 |
Зависимость lg fHfc, от mHcl [ IMAGE ] Зависимость lg. [3] |
На рис. 131 логарифм коэффициента активности соляной кислоты в растворах хлористого натрия при общей ионной силе 1 М и при различных температурах представлен графически в виде функции от моляльности кислоты. Шесть растворителей представляют собой 10 -, 20 -, 30 -, 40 -, 50 - и 60-процентные ( по весу) смеси метилового спирта и воды. [4]
Заштрихованная площадь дает логарифм коэффициента активности второго компонента. [5]
В этом приближении логарифм коэффициента активности растворенного вещества 2 является линейной функцией концентраций остальных компонентов. [6]
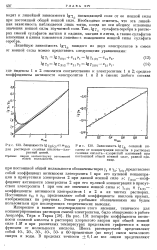 |
Зависимость IgfnTci от mHci [ IMAGE ] Зависимость. [7] |
На рис. 131 логарифм коэффициента активности соляной кислоты в растворах хлористого натрия при общей ионной силе 1 М и при различных температурах представлен графически в виде функции от моляльности кислоты. Шесть растворителей представляют собой 10 -, 20 -, 30 -, 40 -, 50 - и 60-процентные ( по весу) смеси метилового спирта и воды. [8]
В этом приближении логарифм коэффициента активности растворенного вещества 2 является линейной функцией концентрации. [9]
В нем / - логарифм коэффициента активности С при бесконечном разведении, а Е - энергия отталкивания соседних атомов С. Хотя это уравнение неплохо согласуется с данными опыта, применение его к растворам углерода в железе требует дополнительного обоснования. Вычисленная по величине Е ( 3600 кал / г-атом) теплота разбавления настолько мала ( ДЯС 380 кал / г-атом при разведении от 4 4 до 0 атом. [10]
Blg 4 представляют собой логарифмы коэффициентов активности соответственно компонентов 1 и 2 при бесконечно малой их концентрации в растворе. [11]
На рис. 4 представлен логарифм коэффициента активности бензола как функция концентрации ряда солей. [12]
Таким образом, изменение логарифма коэффициента активности вещества, образующего однокомпонентную фазу, пропорционально разности теплосодержания этого компонента в чистом виде и его парциального молярного теплосодержания в растворе. [13]
Эти уравнения выражают зависимость логарифмов коэффициентов активности компонентов от состава раствора в виде некоторых функций, причем входящие в эти уравнения эмпирические постоянные определяются из опытных данных. Уравнения, предложенные разными авторами, различаются видом этих функций и числом эмпирических констант. [14]
Таким образом, изменение логарифма коэффициента активности компонента раствора с давлением при постоянных составе и температуре пропорционально разности парциального молярного объема этого компонента в растворе и его молярного объема в чистом состоянии при той же температуре. Так как приготовление растворов из компонентов обычно сопровождается очень небольшим изменением объема, то разность V n - V n весьма мала. [15]
Страницы: 1 2 3 4