Ацилпероксид
Cтраница 1
 |
Влияние замещения феноксигрупп на хлор при автоокислеиии фосфитов ( инициирование УФ-светом. [1] |
Ацилпероксиды [71-74], перэфиры [75, 76] и гидропероксиды [76] окисляют соединения трехвалентного фосфора преимущественно по ионному механизму. Предложен ионный механизм окисления фосфинов озонидами [ 771: происходит нуклео-фильная атака атомом фосфора по пероксидному кислороду озонид-ной группы. [2]
Ацилпероксиды получают также реакцией солей пероксикарбойовых кислот с хлоран-гидридами карбоновых кислот из пероксикислот и хлорангидридов в присутствии органических оснований. [3]
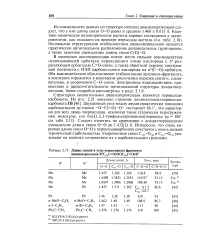 |
J. Длины Связей и углы пероксидного фрагмента диацилпероксидов R C ( ( O OOC ( 2 ( O R2. [4] |
В молекулах ацилпероксидов имеют место сильное взаимодействие несвязываюшей орбитали пероксидного атома кислорода с л - разрыхляющей орбиталъю С-О - связи, а также обратный перенос электронной плотности с НЭП карбонильного кислорода на ст ( С-О) - орбиталь. Оба взаимодействия обусловливают стабилизацию ацилокси-фрагмента, а последнее отражается в некотором увеличении порядка связи и, следовательно, в укорочении С-О - связи. Электронные взаимодействия, приводящие к предпочтительности ортогональной структуры диацилпероксидов, более подробно рассмотрены в разд. Структурно аналогичными диацилпероксидам являются пероксиди-карбонаты. Следует отметить по сравнению с диацилпероксидами уменьшение длины связи О-О до 1.432 ( 2) А. Интересно, что столь короткая длина связи О-О у пероксидикарбоната сочетается с очень низкой термической стабильностью. Укороченные связи С () - О ( 2) и С ( П - О ( Г) указывают на наличие сопряжения их с карбонильными группами. [5]
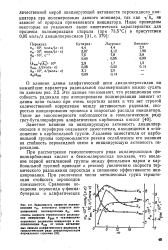
Исследование некоторых ацилпероксидов при низкой ( 77 К) и повышенной ( 95 С) температуре выявило наличие у них люминесценции, что связано с - нахождением в их составе карбонильных групп [ llj. Тате, для пероксида бензоила наибольшая интенсивность Свечения отмечена при возбуждении светом с Д ЗО2 ям в случае пероксида лауроила излучение наблюдается в области - 40О нм. Даже незначительная примесь продуктов фотохимического и термического разложения пероксида лауроила вызывает появление новых полос люминесценции. [6]
Пероксикарбоновые кислоты и ацилпероксиды являются бесцветными жидкостями или кристаллическими веществами, нестабильными и взрывчатыми. [7]
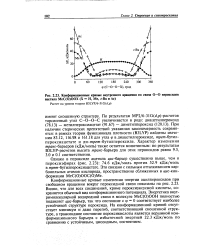 |
Конформационные кривые внутреннего вращения по связи О-О пероксидов ацетила МеС ( О ООХ ( X Н, Me, f - Bu и Ас. [8] |
Конформационные кривые изменения энергии ацилпероксидов при свободном вращении вокруг пероксидной связи показаны на рис. 2.23. Видно, что для всех соединений, кроме пероксиуксусной кислоты, сохраняется обычный вид конформационного потенциала. Энергетика внутримолекулярной водородной связи в молекуле МеС ( О) ООН полностью подавляет мс-барьер, так что состояние с ф 0 соответствует наиболее устойчивой структуре пероксида. На конформационной кривой отсутствует минимум и даже перегиб, соответствующий скошенной структуре, а трансоидное состояние пероксикислоты является вершиной конформационного барьера с избыточной энергией 22.3 кДж / моль по сравнению с устойчивым, цисоидным, состоянием. [9]
Из сравнения электронной структуры ацилпероксида и перокси-эфира со структурой алкилпероксида ( см. ниже) [82] видно, что они являются полярными соединениями. [10]
При рассмотрении гомологического ряда ацилпероксидов фе-нилкарбоновых кислот и бензоилпероксида показано, что введение первой метиленовой группы между фенильным ядром и карбонильной группой приводит к резкому увеличению скорости термического разложения перохсида и снижению эффективности инициирования. При увеличении числа метиленовых групп термическая стойкость пероксидов повышается. [12]
 |
Эфиры алкилфосфоновых кислот R P ( OR a ( O, полученные гемолитическим присоединение. диалкилфосфитов к алкенам. [13] |
Бутилпероксид более эффективен, чем ацилпероксиды или УФ-облучение. [14]
В зависимости от условий разложения ацилпероксидов и пероксиэфиров оно может идти по гемолитическому или гетеролитическому механизму. [15]
Страницы: 1 2