Дофа
Cтраница 1
Дофа и ев производные. L-Дофа, ь - ( 3 4-диоксифенил) аланин, широко применяется при лечении болезни Паркинсона. Она выступает в качестве предшественника дофамина, который вырабатывается в недостаточном количестве у страдающих этой болезнью. Однако D-дофа токсична [73, 74], и ее содержание необходимо контролировать, ввиду того что лечение предусматривает прием больших количеств препарата. [2]
ЛЕВОДОПА [ дофа левопа, допа, ( -) - 3 - ( 3 4-диоксифе-нил) - И-аланин ], крист. [3]
Весьма возможно, что дофа ( продукт окисления тирозина) и является тем субстратом, превращения которого приводят к образованию пигментов кожи, так как свежий кусочек кожи, погруженный в раствор этой аминокислоты, весьма быстро приобретает коричневую окраску. [4]
Тирозин гядроксилирустся до днокснлфенплалапнна [ дофа ], которым может декарбоксилироваться с образованием дофа-амппа [ дшжспфепплэтп. К этому же соединению приводит обходный путь через тнрампп. Дофа-амин пре-вра щается пока еще не выясненным способом в адреналин - гормон коры надпочечников. Последний вместе с норадрепалином ( отличающимся от адреналина отсутствием метмлыюй группы у азота) является частью системы, действие которой особенно ярко проявляется при испуге: вследствие выделения этих гормонов повышается кровяное давление и содержание сахара в крови. Наблюдаемое повышение давления крови аналогично тому, которое наступает при раздражении симпатической нервной системы н может быть вызвано другими аминами сходного строения, получившими вследствие этого название симпатикомиметических. [5]
Синоним этого вещества, принятый в СССР, - дофа. [6]
Под действием тирозиназы тирозин превращается в дисксифенилаланин, или дофу. [7]
В животных тканях ( печень, почки) с наибольшей скоростью декарбоксилируются дофа и цистеиновая кислота, затем глютаминовая кислота ( в ткани мозга), в то время как гистидин и тирозин декарбоксилируются очень слабо. [8]
Дихлофлуанид 489 Диэтиловый эфир 102, 189 Диэтилпропион 471 Додин 490 L-Допа 473 Дофа см. L-Допа Древесина 26 и ел. [9]
К свойствам, которые тесно коррелируют с клинической эффек тивностью антидепрессантов, относятся присущая им адрено -, дофами но-и сероюниносенсибили-зирующая активность. [10]
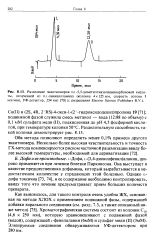
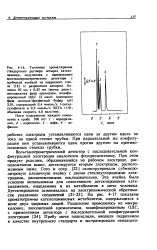
Пики ( содержание каждого компонента в пробе 100 пг): 1 - норадрена-лин, 2 - адреналин, 3 - дофа, 4 - дофамин. [12]
Реакции декарбоксилирования аминокислот наблюдаются не только у микробов, но также в животном и растительном мире. В животном организме обнаружены процессы декарбоксилирования гистидина, тирозина, глютаминовой кислоты, 5-окситриптофана, 3 4-диоксифенилаланина ( дофа) и цистеиновой кислоты. Первые три аминокислоты входят в состав белковой молекулы, три последние ( дофа, 5-окситриптофан и цистеиновая кислота) представляют собой продукты обмена аминокислот - тирозина, триптофана и цистеина. В результате воздействия животных декарбоксилаз на указанные аминокислоты образуются соответствующие амины или новые аминокислоты. [13]
Реакции декарбоксилирования аминокислот наблюдаются не только у микробов, но также в животном и растительном мире. В животном организме обнаружены процессы декарбоксилирования гистидина, тирозина, глютаминовой кислоты, 5-окситриптофана, 3 4-диоксифенилаланина ( дофа) и цистеиновой кислоты. [14]
Однако следует подчеркнуть, что реакция декарбоксилирования аминокислот, несмотря на несомненное физиологическое значение ее, все же не представляет собой основного пути превращения даже тех аминокислот, декарбоксилирование которых в животных тканях доказано с несомненностью. Скорость реакции декарбоксилирования аминокислот в животном организме или весьма мала, как, например, для тирозина, гистидина и триптофана, или, несмотря на большую скорость декарбоксилировавия, реакция все же происходит практически в небольших размерах из-за недостатка субстрата, как, например, для дофа и цистеиновой кислоты, которые образуются в животных тканях в незначительных количествах. [15]
Страницы: 1 2