Масса - атомное ядро
Cтраница 2
Из этой таблицы мы видим, что в данном случае масса атомного ядра довольно сильно влияет на молекулярные свойства, которые, вообще говоря, определяются не ядром, а строением электронной оболочки. Существенное различие молекулярных свойств дейтерия и обычного водорода, не наблюдаемое у изотопов других элементов, объясняется тем, что в данном случае отношение масс ядер несравненно более велико, чем у других элементдв. Все приведенные в таблице числа свидетельствуют о том, что интенсивность молекулярного взаимодействия у дейтерия больше, чем у обычного водорода; соответственно этому дейтерий плавится и закипает при несколько большей температуре, чем обычный водород, требует больших затрат теплоты на плавление и испарение, имеет меньшую упругость пара и меньший мольный объем конденсированных фаз. Энергия междуатомного взаимодействия у дейтерия также несколько превышает энергию взаимодействия атомов обычного водорода, что сказывается в большей устойчивости молекул дейтерия при температурах, вызывающих термическую диссоциацию. [16]
Энергия связи и де - прочно связаны в ядре атома ядерными фект массы атомного ядра силами. [17]
Так как в рассматриваемом случае AW и есть энергия связи ядра S, то масса атомного ядра должна быть меньше суммы масс нуклонов, составляющих ядро, на величину Am, которая называется дефектом массы ядра. [18]
Так как в рассматриваемом случае AW и есть энергия связи ядра 8, то масса атомного ядра должна быть меньше суммы масс нуклонов, составляющих ядро, на величину Am, которая называется дефектом массы ядра. [19]
Хорошее совпадение подобного рода теоретических расчетов с результатами опытов показывает правильность приведенного выше объяснения дефекта массы атомных ядер и подтверждает установленный теорией относительности принцип пропорциональности массы и энергии. [20]
С точки зрения ядерной физики изотопы одного и того же элемента отличаются не только и не столько по массе атомного ядра, сколько по своим свойствам, проявляющимся в ядерных реакциях. [21]
Если эти принципы применимы к молекулам, то силы, удерживающие атомы вместе, почти не будут зависеть от изменений масс атомных ядер, обусловленных изотопным замещением. Однако в случае колебаний, для которых характерно движение атомов с ускорением, инертные массы будут играть большую роль. [22]
Поскольку масса нуклона, выраженная в относительных единицах, очень близка к единице ( масса протона составляет 1 007276, а масса нейтрона - 1 008665), то и масса атомного ядра в относительных единицах близка к целому числу, равному числу нуклонов в ядре. Это число называют массовым числом и обозначают буквой А. [23]
Масса атомного ядра всегда оказывается меньше суммы масс нуклонов. [24]
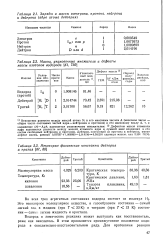 |
Заряды и массы электрона, протона, нейтрона и дейтрона ( ядро атома дейтерия.| Массы, упаковочные множители и дефекты массы изотопов водорода.| Некоторые физические константы дейтерия и трития. [25] |
А) / А называется упаковочным множителем. Дефектом массы атомного ядра называется разность между массой атомного ядра и суммой масс входящих в его состав свободных нейтронов и протонов. Дейтрон, состоящий из протона и нейтрона, имеет дефект массы, равный 1 007597 1 008990 - 2 0141960 002391 единицы массы, или 2 391 ТЕМ. [26]
Упрощения эти в основном сводятся к следующим положениям. Во-первых, большая разница масс атомных ядер и электронов приводит к очень большой разнице в скоростях их движения. [27]
В образовавшейся молекуле атомные ядра не сохраняют относительной неподвижности. В силу того, что масса атомного ядра в тысячи раз превышает массу электрона, движение ядер можно рассматривать как бесконечно медленное по сравнению с движением электронов. Это позволяет считать, что при каждом данном расстоянии г между ядрами успевает установиться стационарное распределение электронной плотности - стационарная тр-функ-ция. [28]
В образовавшейся молекуле атомные ядра не сохраняют относительной неподвижности. В силу того, что масса атомного ядра в тысячи раз превышает массу электрона, движение ядер можно рассматривать как бесконечно медленное по сравнению с движением электронов. Это позволяет считать, что при каждом данном расстоянии г между ядрами успевает установиться стационарное распределение электронной плотности - стационарная - функция. [29]
Эти разности представляют собой количества энергии, нужные для расщепления ядра на соответствующие продукты. Отсюда можно заключить, что масса атомного ядра не равна сумме масс основных составляющих частиц, нейтрона и протона ( с массами 1 0090 и 1 0081 соответственно), поскольку при соединении этих частиц выделилась энергия, и масса уменьшилась эквивалентно этому количеству энергии. Разность между двумя количествами - массой ядра и суммой масс составляющих частиц - является мерой устойчивости ядра. [30]
Страницы: 1 2 3 4