Относительная молекулярная масса - вещество
Cтраница 1
Относительная молекулярная масса веществ с ионной связью находится сложением относительных атомных масс соответствующих элементов с учетом числа атомов каждого элемента. [1]
Относительная молекулярная масса вещества ( УИГ) - это также безразмерная величина, которая выражает массу молекулы в углеродных единицах. Она складывается из относительных атомных масс химических элементов ( Лг), составляющих молекулу. [2]
Относительная молекулярная масса вещества Мг - это число, которое показывает, во сколько раз абсолютная масса молекулы данного вещества больше 1 / 12 части абсолютной массы атома углерода С. [3]
Относительной молекулярной массой вещества называется отношение массы молекулы вещества к / 12 массы атома углерода. [4]
Относительной молекулярной массой вещества называется масса молекулы вещества, выраженная в углеродных единицах. Следовательно, чтобы вычислить относительную молекулярную массу вещества, суммируют относительные атомные массы всех элементов, составляющих молекулу. [5]
Относительной молекулярной массой вещества называется отношение массы молекулы вещества к / 12 массы атома углерода. [6]
Мг - относительная молекулярная масса вещества; п - заряд иона ( абсолютное значение), в виде которого вещество находится в растворе или расплаве. [7]
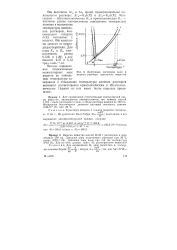 |
Диаграмма состояния воды и водного раствора нелетучего вещества. [8] |
Методы определения относительных молекулярных масс веществ по понижению температуры замерзания и повышению температуры кипения растворов называют соответственно криоскопическим и эбуллиоскопическим, Первый из них имеет более широкое применение. [9]
Как известно, относительная молекулярная масса вещества и относительная атомная масса элемента - это масса молекулы или, соответственно, атома, выраженная в условных атомных единицах. [10]
К; М - относительная молекулярная масса вещества; R - газовая постоянная, эрг / моль град. Уравнение (3.14) выведено в предположении, что испаряющееся в ходе процесса вещество полностью отводится в конденсат. [11]
Полученное значение совпадает с относительной молекулярной массой вещества Е, указанной в условии задачи. Таким образом, простейшая формула вещества Е соответствует его истинной суммарной формуле. [12]
Значение молярной массы численно совпадает с относительной молекулярной массой вещества или относительной атомной массой элемента. [13]
По аналогии с атомной массой используют понятие относительной молекулярной массы вещества. [14]
Из всех представленных в схеме продуктов реакции известна относительная молекулярная масса вещества Н, поэтому идентификацию веществ удобно начать с этого соединения. [15]
Страницы: 1 2 3