Грамм-молекулярная масса
Cтраница 1
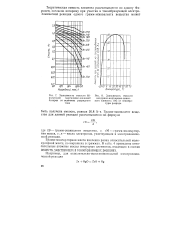 |
Зависимость емкости 60-вольтовой марганцево-цинковой батареи от величины разрядного тока.| Зависимость емкости. [1] |
Грамм-молекулярная масса численно равна относительной молекулярной массе, но выражена в граммах. [2]
Грамм-молекулярная масса FeSCh 152 г, тогда на долю воды приходится 126 г ( 278 - 152), что соответствует 7 молям ( 126: 18) FhO. [3]
Одной грамм-молекулярной массе соответствует 6 02 - 1023 частиц вещества; эту величину часто называют моль. Аналогично-одна формульная масса отвечает 6 02 - 1023 частицам вещества. [4]
При вычислении грамм-молекулярной массы какого-либо вещества находят его молекулярную массу и выражают ее в граммах. [5]
Частное от деления грамм-молекулярной массы ( моля) кислоты на число атомов водорода, которые могут замещаться в рассматриваемой реакции, называется эквивалентной массой кислоты. Аналогично частное от деления грамм-молекулярной массы основания ( моля) на число гидроксильных групп, которые могут замещаться в рассматриваемой реакции, называется эквивалентной массой основания. [6]
Грамм-молекулярный объем находят делением грамм-молекулярной массы на плотность. [7]
Осмоль - это соотношение грамм-молекулярной массы вещества, деленной на число единиц или ионов ( v), образующихся при его растворении. [8]
Следовательно, грамм-эквивалент сульфида соответствует половине его грамм-молекулярной массе. [9]
На примере воды еще раз подчеркнем разницу между грамм-молекулярной массой и грамм-формульной массой, которая по определению составляет для воды 18 015 г. В таком количестве воды содержится несколько меньше, чем один моль НзО, поскольку в воде существуют Н3О, ОН -, Н4О2 и другие частицы. [10]
Опытным путем определено, что показатель преломления этил-ацетата, грамм-молекулярная масса которого 88 11 г и пл. [11]
Молекулярное вращение определяется из выражения [ a ] f грамм-молекулярная масса. [12]
Например, молекулярная масса кислорода О2 равна 32, а грамм-молекулярная масса - 32 г. В отношении веществ, не имеющих молекулярного строения, например Ag2O, CaCO3, HgO и других, вместо молекулярной массы можно говорить о формульной молекулярной массе, как сумме атомных масс атомов входящих в формулу. [13]
Для реально существующих химических веществ вместо грамм-формульной массы лучше употреблять термин грамм-молекулярная масса ( мол. Так, грамм-молекулярная масса Н2 равна его грамм-формульной массе 2 016 г. К NaCl в водном растворе понятие грамм-молекулярной массы неприменимо, поскольку в водной среде такого соединения не обнаружено. Термин грамм-молекулярная масса совершенно справедливо относят к Na ( 23 00 г) и С1 - ( 35 45 г), так как это реально существующие химические частицы; строго говоря, вместо термина грамм-молекулярная масса следовало бы употреблять термин грамм-ионная масса, хотя такое определение встречается редко. [14]
Грамм-моль Na2SO4 хНгО ( 142 18) г, где 142 г - грамм-молекулярная масса Na2SO4, 18 г - грамм-молекулярная масса НЮ. [15]
Страницы: 1 2