Байуотер
Cтраница 1
Байуотер [1256], Брокхаус и Енкель [1257], исследовали кинетику термической деструкции полиметилметакрилата в вакууме при 100 - 200 и 250 - 350s и обнаружили, что скорость реакции при всех температурах быстро падает по мере увеличения глубины разложения, причем величина начальной скорости реакции тем выше, чем ниже молекулярный вес исходного полимера; полная энергия активации реакции деструкции равна - 47 ккал / моль ( для полиметилметакрилата с мол. Авторы предполагают, что распад полиметилметакрилата происходит по цепному механизму. [1]
Байуотер [13] считают ее неправдоподобной. [2]
Кови и Байуотер [37] предложили метод, аналогичный методу Штокмайера и Фиксмана, для оценки невозмущенных размеров по коэффициентам трения. [3]
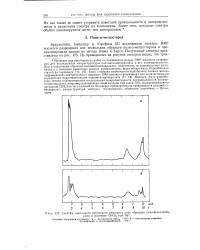 |
Спектры протонного магнитного резонанса двух образцов поли-а-метилстирола в растворе СНС13 при 80. [4] |
Браунштейн, Байуотер и Уорсфолд [5] исследовали спектры ЯМР высокого разрешения для нескольких образцов поли-а-метилстирола и проанализировали данные по методу Бовея и Тирса. [5]
Па основании этой схемы Баксеидаль, Байуотер и Эпанс [314] приходят к выводу, который был подтвержден экспериментально, что число молей полимера, образовавшихся к концу реакции, равно числу молей перекиси водорода, присутствующей в начале. [6]
Следует заметить, как это было сделано Талат-Эрбеном и Байуотером [44], что предположение Уоллинга о том, что разница между измеренными количествами захваченных радикалов и выделившегося азота представляет собою эффект клетки, не доказано. Тем не менее возможно, что низкая эффективность инициирования этими соединениями в растворах четыреххлори-стого углерода связана с эффектом клетки. Так, согласно Боуну и Меллишу [13], в этом растворителе скорость образования радикалов, измеренная при помощи акцептора а, а - ди-фенил-р-пикрилгидразила, значительно ниже, чем в растворе бензола, хотя общие скорости распада в бензоле и четырех-хлористом углероде близки между собою. Такое заключение согласуется с результатами исследования Лэмпа и Нойеса по фотолизу йодистого аллила и йода в четыреххлористом углероде, гексане и гексахлорбутадиене. [7]
Для реакции типа CH3 HR [ CH3 - HR ] - - CH4 R, а также для подобных ей реакций отрыва Н атома атомами Н и атомами галогенов был проведен ряд расчетов. Байуотер и Роберте [9] провели подробное сравнение таких реакций для ряда соединений; полученные данные позволяют более детально проследить за изменением энтропии активации. В табл. XII.3 приведены величины вычисленных стандартных ( при 300 К и 1 атм) молярных энтропии поступательного и вращательного движений комплексов Н или СН3 с RH и изменения стандартной энтропии в реакциях H HR t H2R, CH3 HR CH4R ( пренебрегая колебательным движением), найденные этими авторами. [8]
Для реакции типа CH3 HR; [ CH3 - HR ] - - CH4 R, а также для подобных ей реакций отрыва Н атома атомами Н и атомами галогенов был проведен ряд расчетов. Байуотер и Роберте [9] провели подробное сравнение таких реакций для ряда соединений; полученные данные позволяют более детально проследить за изменением энтропии активации. К и 1 атм) молярных энтропии поступательного и вращательного движений комплексов Н или СН3 с RH и изменения стандартной энтропии в реакциях H HR 2lH2R, CH3 HR CH4R ( пренебрегая колебательным движением), найденные этими авторами. [9]
Хотя кинетика распада динитрила а, а - азодиизомасляной кислоты проста, относительно природы последующих реакций имеются некоторые сомнения. Талат-Эрбен и Байуотер [44] показали, что при его распаде при 80 образуется нестойкий промежуточный продукт, концентрация которого достигает максимальной величины через 100 мин. [10]
Этот раздел был бы неполным без ссылки на возможно самую известную и широко применяемую схему с разбиваемыми перегородками. Установка такого тина, которой пользуются большинство исследователей в области изучения процессов анионной полимеризации, была создана ipyimoft Шварца ( Сиракузы, США), а затем модифицирована усилиями исследователей из групп Байуотера, Сигвалта, Дж. [12]
Реакции алканов, сенсибилизированные ртутью, исследованы при повышенных температурах. Результаты, по-видимому, предсказываются на основе термической стабильности и реакционной способности радикалов, возникающих при первичном акте. Однако Байуотер и Стейси [83] ( 1951 г.) нашли, что в сенсибилизированных реакциях бутана и изобутана при температурах выше 260 появляются продукты разложения и-бутилового и изобутилового радикалов. [14]
Поэтому можно ожидать, что энтропия активации для молекул углеводородов, еще больших, чем изобутан, должна лишь немногим превышать величину, полученную для изобутана. Возможная ошибка вычислений не превышает величин 2 - 3 кал / моль - град для изменения энтропии, что соответствует изменению предэкспоненциального множителя приблизительно в 3 раза. Исходя из имеющихся в литературе данных по реакциям отрыва атома Н, Байуотер и Роберте нашли, что рассчитанные значения предэкспоненциального фактора вполне удовлетворительно совпадают с экспериментальными данными, отличаясь от последних не более чем в 10 раз. [15]
Страницы: 1 2

