Одновалентная медь
Cтраница 1
Одновалентная медь не образует комплекса с виннокислой солью. [1]
Одновалентная медь образует несколько типов полиядерных комплексов, в которых четыре атома Си лежат в вершинах тетраэдра. [2]
Одновалентная медь не образует комплекса с виннокислой солью. [3]
Одновалентная медь ( с заполненной оболочкой из 18 электронов) не является ни переходным, ни сильно электроположительным металлом; на этом основании можно ожидать, что она образует ряд ковалентных моноалкильных соединений. Это вещество при 80 разлагается на медь и бифенил, а при гидролизе дает бензол и медь. Его можно рассматривать либо как ионное вещество, подобное фенилнатрию, либо как истинно ковалентное арильное соединение, подобное аналогичным соединениям ртути; однако не было сообщений об экспериментах, позволяющих сделать выбор. [4]
Одновалентная медь в присутствии азотной кислоты быстро окисляется до двухвалентной. В результате этого концентрация ионов нитрозила возрастает, что приводит к увеличению скорости стадий нитрозирования. [6]
Одновалентная медь образует с ионами Вг более устойчивые комплексы, чем с ионами СГ. Даже при меньшей концентрации ионов Вг - второй скачок потенциала настолько мал, что не имеет практического значения. Потенциал Си1 / Си1 становится более положительным в присутствии ионов ВГ, чем в присутствии ионов СГ. Вследствие этого скачок потенциала в первой точке эквивалентности больше в бромиднои среде, чем в хлоридной, а воспроизводимость и точность результатов одинаково хороща в обоих случаях. В общем, бромидная среда не имеет каких-либо практических преимуществ по сравнению с хлоридной средой при определении меди. [7]
Одновалентная медь входит в состав комплексных катионов, анионов и комплексов типа неэлектролитов. [8]
 |
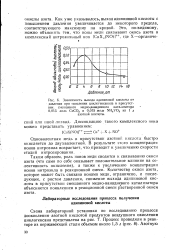
Зависимость выхода адипиновой кислоты от давления при окислении циклогексанола в присутствии смешанного медно-ванадиевого катализатора 0 015 моль СиСО3 и 0 015 моль NH4VO3 на 1 л азотной кислоты. [9] |
Одновалентная медь в присутствии азотной кислоты быстро окисляется до двухвалентной. В результате этого концентрация ионов нитрозила возрастает, что приводит к увеличению скорости стадий нитрозирования. [10]
Одновалентная медь образует я-комплексы с ацетиленом, моно - и диза-мещенными ацетиленами. [11]
Одновалентную медь генерируют, как правило, в солянокислых растворах с концентрацией 0 5Л1 НС1 путем восстановления Си2 на платиновом катоде. [12]
Соединения одновалентной меди образуют устойчивые комплексы с ацетонитрилом. [13]
Соединения одновалентной меди легко окисляются воздухом до соединений двухвалентной меди. Соединения двухвалентной меди более важные и более распространенные, чем соединения одновалентной меди. Соли двухвалентной меди имеют синюю или зеленую окраску. Все соли меди в той или иной мере ядовиты. [14]
Соединения одновалентной меди образуют устойчивые комплексы с ацетонитрилом. [15]
Страницы: 1 2 3 4