Мера - неупорядоченность
Cтраница 3
Уравнение (17.6) полностью определяет изменение энтропии в математическом отношении, однако следует разобраться в физическом смысле этой вновь введенной функции состояния. Энтропия системы является мерой неупорядоченности ее состояния. Согласно уравнению (17.6), это означает, что если в систему поступает тепловая энергия, она обусловливает повышение неупорядоченности. [31]
Наиболее простое объяснение вытекает из признания связи энтропии с неупорядоченностью движения молекул. Действительно, энтропию можно трактовать как меру неупорядоченности системы. При такой трактовке возрастание энтропии характеризует увеличение неупорядоченности системы. Выравнивание температур тел при теплообмене напоминает, что превратить порядок в беспорядок просто, но нелегко обратить этот процесс. Легко нарушить порядок, при котором сахар и соль лежат порознь в банках, смешав их вместе, но практически весьма сложно вернуть их к прежнему порядку. Точно так же легко превратить электрическую энергию в тепло, но практически невозможно превратить это же тепло обратно в прежнее количество электроэнергии. [32]
Энтропия при этом играет роль функции Ляпунова в близких по смыслу задачах теории устойчивости. Как мы знаем, энтропия является мерой неупорядоченности движений в системе, и потому ее возрастание с течением времени говорит о диссипативном характере процесса в системе. [33]
По нашему мнению, между каталитической активностью и упомянутым выше физическим состоянием не может существовать никакой непосредственной связи. Хотя, конечно, проводимость является мерой электронной неупорядоченности, она, однако, ничего не говорит о характере неупорядоченности катализаторов. В качестве примера можно указать на случай одинаковых значений электропроводности р - и л-проводящих окислов при различии их каталитических свойств. [34]
Энтропия является функцией состояния, так как, подобно внутренней энергии и энтальпии, зависит только от конечного и начального состояний и не зависит от пути процесса. Она может вместе с этим служить мерой неупорядоченности системы, так как связана с вероятностью. [35]
Отсюда следует, что энтропия является мерой неупорядоченности системы и самопроизвольно идущие при определенных уело-виях процессы, связанные с уменьшением порядка в распределении частиц, характеризуются увеличением энтропии. [36]
Фазовый переход - это давно известный и наиболее полно изученный процесс возникновения и изменения степени упорядоченности в замкнутых, изолированных системах, состоящих из конечного числа однородных элементов. Одной из основных величин, которая характеризует меру неупорядоченности системы, является энтропия. Эта величина логарифмически растет с увеличением числа возможных состояний в системе. Согласно второму закону термодинамики, в изолированной системе через определенное время будет достигнуто термодинамическое равновесие, которому отвечает максимальное значение энтропии. Иными словами, в замкнутых системах, выведенных из положения термодинамического равновесия и характеризующихся определенным числом состояний, с течением времени будет достигнуто состояние с меньшей степенью упорядочения. Простейшим примером такого процесса может служить, например, растворение сахара в стакане чая. Особенно важно, что подобные процессы протекают только в одну сторону, а обратные процессы невозможны. [37]
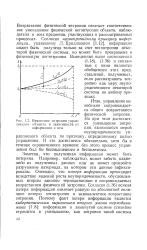 |
Изменение энтропии управляемого объекта в зависимости от информации о нем. [38] |
Итак, управление неизбежно сопровождается общим возрастанием физической энтропии. Но при этом достигается уменьшение энтропии, являющейся мерой неупорядоченности управляемого объекта по признаку, определяемому целью управления. И это достигается обязательно, хотя бы в течение ограниченного времени: без этого процесс управления был бы бессмысленным и бесполезным. [39]
В зависимости от метода измерения рассогласования энтропия может быть непрерывной или квантованной, ее можно оценить либо по сравнению с постоянным рассогласованием, либо по отношению к некоторой области. Таким образом, функция целевой энтропии позволяет определить меру неупорядоченности функционирования системы в отношении достижения поставленной цели управления. Для определения ценности управляющей информации нужно рассмотреть разность целевых энтропии до и после замыкания канала управления на объект управления. [40]
Планк дополнил тепловую теорему Нернста следующим положением: Энтропия чистых кристаллов при температуре абсолютного нуля равна нулю. Теоретическое обоснование этого постулата выводится из квантовой статистики, по которой энтропия есть мера неупорядоченности. [41]
Когда энтропия выводится из второго закона термодинамики, она не получает очевидной интерпретации на молекулярном уровне. Однако австрийский физик Людвиг Больцман ( 1844 - 1906) показал в 1877 г., что энтропия имеет основополагающее значение для понимания молекулярных явлений: она является мерой неупорядоченности в молекулярной системе. Больцман показал, что энтропия S связана с числом различных микроскопических способов реализации конкретной макроскопически определенной и наблюдаемой ситуации. [42]
Состояние веществ и их систем характеризуют рядом параметров. Энтропия s представляет собой меру неупорядоченности микрочастиц в макроскопической системе веществ. [43]
В выражении (1.3) член ДЯР, как мы уже знаем, может быть положительным или отрицательным. Однако и величина ГД51 также может принимать положительные и отрицательные значения. Как известно, энтропия является мерой неупорядоченности, хаотичности системы, степень которых возрастает с переходом ионов в раствор. [44]
В настоящее время энтропия трактуется как мера неупорядоченности состояния системы. [45]
Страницы: 1 2 3 4