Меркурирование - бензол
Cтраница 1
Меркурирование бензола в уксусной кислоте является реакцией второго порядка, первого порядка по ароматическому углеводороду и первого порядка по концентрации иона ртути. Реакция заметно катализируется хлорной кислотой и перхлоратом натрия, ион хлора ее замедляет. [1]
Меркурирование бензола ртутной солью тринитрометана происходит в сравнительно мягких условиях ( 5 час. Этот эффект вызван удалением воды от иона ртути. [2]
Меркурирование бензола [116, 117], повидимому, происходит по схеме XIX-XXI. Поэтому очевидно, что меркурирование фурана подпадает под общие выводы, данные выше, признающие положительный характер ртутного заместителя. [3]
Реакция меркурирования бензола является наиболее медленной стадией и определяет скорость всего процесса превращения бензола в динитрофенол. В оптимальных условиях в 1 л 50 % - ной кислоты при 55 в азотнокислую фенил-ртуть превращается за 3 часа около 0 7 г-мол бензола. [4]
Получается меркурированием бензола ацетатом ртути с катализаторами - трифторидом бора или фторидом сурьмы. [5]
Константу равновесия меркурирования бензола в условиях окислительного нитрования определять трудно, поскольку азотная кислота при этом находится частично в ионизированной и частично в неионизированной форме. [6]
Это доказывает обратимость реакции меркурирования бензола действием перхлората ртути в хлорной кислоте. [7]
Гладко и с хорошим выходом ( до 80 %) идет Меркурирование бензола, действием азотнокислой ртути в присутствии окиси ртути и сульфата кальция и в отсутствии воздуха. [8]
Суперароматическая природа ферроцена проявляется также в том, что его меркурирование, в отличие от меркурирования бензола, гладко осуществляется в мягких условиях: действием уксуснокислой ртути при комнатной температуре в эфирно-спиртовом растворе. Хлористая ферроценилртуть - оранжево-желтое кристаллическое вещество, плохо растворимое в эфире, бензоле, метиловом и этиловом спиртах; кристаллизуется из ксилола и бутилового спирта. Дихлормеркурферро-цен - светло-желтое порошкообразное вещество; не плавится, слабо растворяется в кипящих бутиловом спирте, дихлорэтане и ксилоле, несколько лучше - в горячих диоксане, этиленгликоле и циклогексаноле. [9]
Ртутные производные обычно получают обработкой ароматического соединения ацетатом ртути. Примером служит меркурирование бензола, протекающее с контролируемой скоростью при добавлении ацетата ртути в ледяной уксусной кислоте к бензолу. [10]
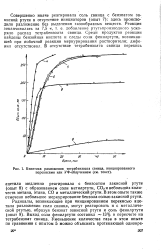 |
Кинетика разложения тетрабензоата свинца, инициированного перекисями или УФ-облучением ( текст. [11] |
В этом опыте также отмечено небольшое меркурирование бензола солью закисной ртути. [12]
Эта реакция протекает при температуре 100 - 110 С в автоклаве. В качестве побочных продуктов в небольших количествах получаются продукты более глубокого меркурирования бензола. [13]
В качестве побочных продуктов образуется небольшое количество полимеркурированных производных бензола, которые легко отделяются от фенилмеркурацетата вследствие плохой растворимости в горячей воде и углеводородах. Однако при проведении реакции в мягких условиях и при большом избытке бензола эти побочные процессы могут быть сведены до минимума. Обычно меркурирование бензола осуществляют при температуре не выше 130 С ( предпочтительно не выше 100 С), а в присутствии некоторых катализаторов, как, например, трехфтористого бора, температуру реакции можно снизить до 20 - 40 С. [14]
В качестве побочных продуктов образуется небольшое количество полимеркурированных производных бензола, которые легко отделяются от фенилмеркурацетата вследствие плохой растворимости в горячей воде и углеводородах. Однако при проведений реакции в мягких условиях и при большом избытке бензола эти побочные процессы могут быть сведены до минимума. Обычно меркурирование бензола осуществляют при температуре не выше 130 С ( предпочтительно не выше 100 С), а в присутствии некоторых катализаторов, как, например, трехфтористого бора, температуру реакции можно снизить до 20 - 40 С. [15]
Страницы: 1 2