Молярная дробь
Cтраница 3
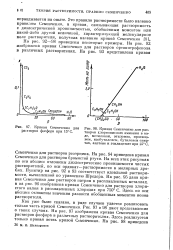 |
Кривая Семенченко для растворов хлориокислого аммония в воде, метиловом, этиловом, пропило-вом, изобутиловем, бутиловом спиртах, ацетоне и этилацетате при 25 С. [31] |
Семенченко для растворов рсзорпина. На рис. 94 приведена кривая Семенчснко для растворов бромистой ртути. На всех этих рисунках по оси абсцисс отложены диэлектрические проницаемости чистых растворителей, по оси ординат-растворимости в молярных дробях. Пунктир на рис. 92 и 93 соответствует идеальной растворимости, вычисленной по уравнению Шредера. На рис. 95 дана кривая Семенченко для растворов натрия в расплавленных металлах, а на рис. 96 изображена кривая Семенченко для растворов хлористого калия в расплавленных хлоридах при 750 С. Здесь по оси абсцисс отложены значения разности обобщенных моментов ионов растворителя. [32]
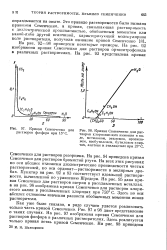 |
Кривая Семенченко для растворов хлорнпкислого аммония в воде, метиловом, этиловом, пропило-вом, изобутиловом, бутиловом спиртах, ацетоне и этилацетате при 25 С. [33] |
Семенченко для растворов резорцина. На рис. 94 приведена кривая Семенченко для растворов бромистой ртути. На всех этих рисунках по оси абсцисс отложены диэлектрические проницаемости чистых растворителей, по оси ординат-растворимости в молярных дробях. Пунктир на рис. 92 и 93 соответствует идеальной растворимости, вычисленной по уравнению Шредера. На рис. 95 дана кривая Семеиченко для растворов натрия в расплавленных металлах, а на рис. 96 изображена кривая Семснченко для растворов хлористого калия в расплавленных хлоридах при 750 С. Здесь по оси абсцисс отложены значения разности обобщенных моментов ионов растворителя. [34]
АЯт - - теплота реакции при Т для газов, находящихся в стандартном состоянии при постоянном давлении. Парциальные величины пишутся прописной буквой с индексом, характеризующим компонент, и с чертой наверху. Больцмана, Кс Кр К К К - константы равновесия, выраженные соответственно через концентрации, парциальные давления, летучести, молярные дроби, коэфициенты активности. [35]
Во многих случаях с уменьшением концентрации раствора закономерности, которым подчиняются свойства раствора, становятся более простыми. Поэтому различают концентрированные, разведенные и предельно ( или бесконечно) разведенные растворы. Различие между этими группами растворов также не является строго определенным. Обычно, если концентрация какого-либо из компонентов, выраженная в молярных дробях, меньше 0 05, раствор считается разведенным по отношению к этому компоненту. Предельно разведенные растворы представляют собой экстремальный случай. Предельно или бесконечно разведенный раствор можно определить как такой раствор, в котором концентрация растворенного вещества меньше любой конечной величины. Законы, управляющие поведением предельно разведенных растворов, наиболее просты. Это - предельные законы, выполняющиеся тем точнее, чем более разбавлен раствор. Поэтому предельно разведенные растворы занимают в учении о растворах особое место, свойства их отличаются не только от свойств концентрированных, но и от свойств сравнительно разведенных растворов. [36]
Во всех рассмотренных здесь случаях предполагалось, что молекулы / - - мера не могут образовывать замкнутых колец. Однако значения термодинамических функций, вычисленные для растворов кольцеобразных молекул / - - мера, мало отличаются от значений тех же функций, вычисленных для цепочечных молекул r - мера. В табл. 27 сравнены значения SM / R для растворов тримеров в мономере. В первой графе содержатся объемные дроби тримера р, во второй графе - молярные дроби тримера х, в третьей и четвертой графах - значения SMjfi, вычисленные по уравнению (9.145) для цепочечного тримера при z 12 и z 6, в пятой графе - значения SM IR, вычисленные для тримера, молекулы которого образуют равносторонний треугольник, причем все три сегмента в молекуле одинаковы. [37]
Страницы: 1 2 3