Амис
Cтраница 1
Амис [19] предположил, что в случае диполь-дипольных взаимодействий влияние диэлектрической проницаемости на скорость реакции описывается следующими уравнениями, в которых отброшены все члены, содержащие в знаменателе степени расстояния между центрами зарядов в дипольнои молекуле выше третьей. [1]
Амис [33] опубликовал данные об образовании синтетических цеолитов типа анальцима и морденита в системе Na20 - А1203 - Si02 - H20 при 250 - 300 С. [2]
Амис и Джаффе предполагают далее, что Ф ( г) положителен для тех расстояний, на которых происходит образование промежуточного комплекса X, и не зависит от диэлектрической проницаемости растворителя. Это последнее предположение разумно, так как на расстоянии, необходимом для образования промежуточного комплекса, диэлектрические свойства растворителя, по-видимому, не имеют значения. [3]
Вывод Амиса ( см., например, [2]) с применением выражений (11.43) и (V.92) для неизодиэлектрических условий, хотя и приводит к той же формуле, однако является некорректным. [4]
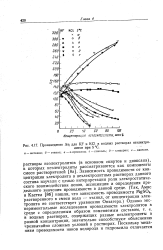 |
Произведение Лт ] для KF и КС1 в водных растворах неэлектролитов при 5 С... - - а - метанол. б - этанол. в - н-пропанол. г - гликоль. д - глицерин. е - диоксан. [5] |
Так, Амис и Кастел [86] нашли, что зависимость проводимости MgSO4, растворенного в смеси вода - этанол, от концентрации электролита не соответствует уравнению Онзагера. [6]
По мнению Амиса [5], данные по реакции электронного обмена можно объяснить, предполагая, что перенос электрона между реагентами осуществляется мостиковым механизмом и что здесь происходит избирательная сольватация активированного комплекса компонентой растворителя с более высокими диэлектрическими свойствами в условиях полного диэлектрического насыщения. Эта теория более подробно будет рассмотрена позднее. [7]
Цеолит типа клиноптилолита синтезирован Амисом [33], изучавшим кристаллизацию гелей, полученных из смесей гидроокиси лития, гидроокиси алюминия и силикагеля. [8]
 |
Радиусы и теплоты удаления ионов из раствора. [9] |
Переменная ЕЛ была названа Амисом [4, 5] изодиэлектрической энергией активации. [10]
Это уравнение было использовано Амисом и Джаффе при анализе экспериментальных данных по инверсии сахарозы и мутаротации глюкозы в соляной кислоте. Катализируемая кислотой инверсия сахарозы, использованная при проверке следствий из уравнения (2.50), была изучена [9] в водно-диоксановых смесях, а катализируемая кислотой мутаротация глюкозы была изучена Диасом и Хиллом [10] в смесях воды с метанолом. [11]
Используя приближение кулоновского взаимодействия, Амис [ На ] получил для зависимости In k от l / D уравнение, идентичное уравнению Скэтчарда. [12]
В предлагаемой вниманию советского читателя монографии Амиса систематизирован и обобщен большой теоретический материал в сопоставлении с известными экспериментальными данными. В монографии последовательно рассматриваются вопросы влияния растворителя на реакции между нонами, между ионами и полярными молекулами, а также - на реакции электронного обмена. Отдельная глава посвящена разбору корреляционных уравнений ( уравнения Бренстеда, Гаммета, Тафта и др.) которые получили широкое распространение при обработке экспериментальных данных. В монографии на конкретных примерах рассматриваются также такие важные вопросы, как влияние избирательной сольватации, клеточного эффекта и водородных связей на скорость и механизм различных химических реакций. [13]
Температурный коэффициент для электропроводности, найденный Педерсеном и Амисом [21], получен из уравнения Он-загера и поэтому включает электростатические представления так же, как и влияние растворителя. Влияние растворителя несомненно является результатом зависимости диэлектрической проницаемости и вязкости растворителя от температуры. [14]
Эта теория, как было показано Рочом и Амисом [32], весьма чувствительна к типу заряда исследуемого электролита. [15]
Страницы: 1 2