Свободные координационные места
Cтраница 2
Стеклование в кислой области в концентрированных растворах, вероятнее всего, происходит за счет дополнительной координации центральным атомом комплексного аниона фосфоновых групп [ РО ( ОН) 21 другого лиганда, свободные координационные места которого предоставляются еще одному катиону. Несомненно, в образовании таких комплексных ассоциатов принимают участие водородные связи, но их наличие не может быть единственным и главным объяснением подобного явления. [16]
Стеклование в кислой области в концентрированных растворах, вероятнее всего, происходит за счет дополнительной координации центральным атомом комплексного аниона фосфоновых групп [ РО ( ОН) 2 ] другого лиганда, свободные координационные места которого предоставляются еще одному катиону. Несомненно, в образовании таких комплексных ассоциатов принимают участие водородные связи, но их наличие не может быть единственным и главным объяснением подобного явления. [17]
Анализ кристаллических структур комплексов белков с металлами показал, что аминокислотные комплексы металлов имеют октаэдрическое строение, причем два остатка аминокислоты связаны с центральным атомом металла амино - и карбоксильными группами, а свободные координационные места заняты водой. Особой устойчивостью отличаются комплексы с аминокислотами, имеющими функциональные боковые цепи, как, напри-ме Р, гистидин, азот имидазола в котором образует дополнительную связь с центральным атомом. [18]
Этот процесс можно представить как передачу двух электронов металла молекуле X - Y, в результате чего происходит разрыв связи в ней и образование двух лигандов ( Х: - и Y: -), которые занимают свободные координационные места в новом комплексе. [19]
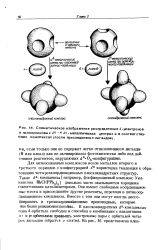 |
Схематическое изображение распределения rf - эпектронов в низкоспиновых ds - и rf6 металлических центрах и в соответствующих комплексах ( после присоединения лигандов. [20] |
Для низкоспиновых комплексов ионов металлов второго и третьего периодов с конфигурацией ds характерна тенденция к образованию четырехкоординационных плоскоквадратных структур Такие ds - комплексы [ например, фосфинродиевый комплекс Уил-кинсона RhCl ( PPh3) 3 ] довольно часто оказываются хорошими гомогенными катализаторами Они имеют свободные координационные места и присоединяют другие реагенты, переходя в пятикоор-динационные комплексы. [21]
Весьма похожий метод разработали Латтерелль и Уолтон [144] для разделения химически подобных аминов. Они использовали Ni-форму смолы, содержащей карбоксильные группы, а именно свободные координационные места связанного никеля для хроматографического обмена лигандов ( ср. [22]
Этот реагент флуоресцирует в кислой среде голубым цветом, однако в присутствии перекиси водорода и следов железа происходит каталитическое разрушение реагента и флуоресценция исчезает. Механизм реакции следующий: образующийся в кислой среде комплекс реагента с железом имеет свободные координационные места, за счет этого образуется смешанный комплекс стильбексон - железо - перекись водорода. Этот комплекс термодинамически неустойчив, происходит окисление реактива по месту двойной связи и флуоресценция раствора исчезает. Реакция протекает по уравнению первого порядка относительно реактива. Чувствительность реакции составляет 0 0025 мкг железа в 5 мл раствора. [23]
Особое внимание следует обратить на способность этих соединений образовывать прочные комплексы с Be. Изучение механизма комплексообразования показало, что оно обусловлено взаимодействием Be только с фосфоновыми группировками; N иминоалкилфосфоновых групп в комплексообразо-вании не участвует. Свободные координационные места в комплексах могут быть заполнены другими катионами, при этом образуются полиядерные комплексы с двумя координационными центрами, в роли которых выступают два разных катиона. [24]
По сдвигу полос в спектрах поглощения эквимолярных комплексов установлено [199], что ДТПА с редкоземельными элементами проявляет дентатность, равную шести, в координации участвуют 3 атома азота и 3 атома кислорода карбоксильных групп. Две карбоксильные группы не входят во внутреннюю сферу комплекса. Вероятнее всего, второй ион металла занимает оставшиеся свободные координационные места лиганда, образуя при этом внешнюю сферу. Подтверждением этого является возрастание lg / ca с увеличением дентатности и меньшая разница в константах присоединения первого и второго катионов. [25]
По сдвигу полос в спектрах поглощения эквимолярных комплексов установлено [199], что ДТПА с редкоземельными элементами проявляет дентатность, равную шести, в координации участвуют 3 атома азота и 3 атома кислорода карбоксильных групп. Две карбоксильные группы не входят во внутреннюю сферу комплекса. Вероятнее всего, второй ион металла занимает оставшиеся свободные координационные места лиганда, образуя при этом внешнюю сферу. Подтверждением этого является возрастание lg &2 с увеличением дентатностии меньшая разница в константах присоединения первого и второго катионов. [26]
Таким образом, пятикоординационные Й6 - комплексы или че-тырехкоординационные - комплексы должны быть активными катализаторами, тогда как шестикоординационные с. Наличие длительных индукционных периодов или необходимость термического инициирования реакции часто указывают на отщепление лиганда, приводящее к образованию активных катализаторов. Механизм действия каталитических ядов, например соединений фосфора и серы, а также окиси углерода, заключается в том, что они занимают свободные координационные места. Последние могут также блокироваться мостиковыми лигандами. Аналогичные процессы, по-видимому, протекают при отравлении активных центров на поверхности гетерогенных катализаторов. [27]
Таким образом, пятикоординационные - комплексы или че-тырехкоординационные - комплексы должны быть активными катализаторами, тогда как шестикоординационные d6 - и пятикоординационные - комплексы не будут проявлять каталитической активности до тех пор, пока не потеряют лиганд. Наличие длительных индукционных периодов или необходимость термического инициирования реакции часто указывают на отщепление лиганда, приводящее к образованию активных катализаторов. Механизм действия каталитических ядов, например соединений фосфора и серы, а также окиси углерода, заключается в том, что они занимают свободные координационные места. Последние могут также блокироваться мостиковыми лигандами. [28]
Такие соединения экстрагируются, как правило, только в присутствии большого избытка реагента. Методы изомолярных серий, молярных отношений и отношения наклонов приложимы к ним, по-видимому, не всегда. Действительно, аддукты указанного вида характерны для катионов, координационное число которых превышает их удвоенный заряд, в результате чего у образующегося нейтрального комплекса, скажем U02A2, остаются свободные координационные места. [29]
Активатор в этой реакции выполняет сразу несколько функций. Во-первых, он удерживает катализатор в растворе при том значении рН среды, при котором соль же-леза ( 111) была бы полностью гидролизована. Во-вторых, триэтилентетрамин, присутствуя в координационной сфере катализатора, обеспечивает присоединение к последнему субстрата бидентатным способом. Структура этого активатора такова, что он не может координироваться катализатором иначе, как только оставляя два свободных координационных места в г ыс-положении друг относительно друга. [30]
Страницы: 1 2 3