Хлористый металл
Cтраница 2
Указанное выше соотношение не ограничивается растворами хлористых металлов, а идет почти так же и далее, потому что НВг ( D 1 030 M81), LiBr ( D l 032, M87), NaBr ( D l 043, М103), КВг ( 0 1 047, М119), MgBr2 ( D 1 081, М184), СаВг2 ( D 1 088, М200), ZnBr2 ( D 1 106, М225), SrBr2 ( D l 115, M247), CdBr2 ( Dl120, M272), BaBr2 ( D 1 133, М297), а также йодистые металлы от JH ( D 1 049, M128) до BaJ2, даже йодноватая кислота HJO3 ( D 1 081, M176), AgN03 ( D l 076, M170) и многие другие вещества в растворах представляют такую же степень зависимости плотности от частичного веса, какая замечается для, хлористых металлов. [16]
Это соединение происходит при действии раствора хлористых металлов на другие растворимые основные соли свинца. [17]
Хлористый алюминий А12С16 получается, как и другие подобные хлористые металлы ( напр. Получается возгонкою, потому что весьма летуч. Он представляет кристаллическую, легкоплавкую массу, расплывающуюся на воздухе, легко растворяющуюся в воде с отделением большого количества тепла. При испарении такого раствора выделяется соляная кислота и водная окись алюминия. Способность же к соединению типа А1Х3 с другими частицами видна в соединении А1С13 со многими другими соединениями хлора - так, напр. Соединение хлористого алюминия с хлористым натрием AlNaCl весьма легкоплавко и гораздо более постоянно на воздухе, чем сам хлористый алюминий. Оно, очевидно, того же типа, как квасцы. [18]
Для извлечения остатков марганца, никкеля и других хлористых металлов из находящегося в верхнем шаре раствора, к нему приливают 10 мл насыщенной эфиром соляной кислоты ( плотн. После разделения жидкости в обош шарах на два слоя остатки других металлов вместе с небольшим количеством хлорного железа перешли в верхнем шаре из эфирного ело в солянокислый. В нижнем шаре, наоборот, хлорное железо, присутство вавшее в солянокислом растворе в количестве, самое большее, 1 - 2 мг перешло в свежий эфир. Соответственно этому дальнейшие взбалтыванш имеют целью извлечение из эфирного раствора хлорного железа, находя щегося в верхнем шаре, остатков других хлористых металлов; с друго. [19]
В процессе получения S35 при облучении дейтронами кристаллов хлористых металлов радиоактивная сера образуется в виде элементарной или отрицательно двухзарядной. Затем она вступает в реакцию с адсорбированным в кристаллах кислорсдом, образуя S0a, или с хлором, образуя хлориды серы. Получение хлоридов серы наблюдается и при облучении четыреххлористого углерода нейтронами. [21]
Предложенный механизм включает образование НС1 за счет пирогидролиза хлористых металлов. Аналогичные реакции, вероятно, имеют место для бромидов и иодидов. Фториды относительно стабильны, поэтому они не подвергаются гидролизу. Предположили, что это является причиной их инертности в отношении растрескивания. Абсорбция титановыми сплавами водорода при экспонировании их в хлористых солях при повышенных температурах установлена достаточно определенно [9], при этом указано, что количество абсорбированного водорода пропорционально количеству влаги, участвующей в реакции. [22]
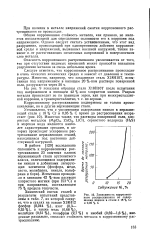 |
Зависимость коррозионного растрескивания от содержания никеля в стали с 18 % Сг и 0 05 % С. [23] |
Известно также, что растворы поваренной соли, хлористых металлов ( MgCb, ZnCb, LiCl), сернистого водорода ( H2S) и морская вода являются наиболее характерными средами, в ко-торых происходит ускоренное растрескивание нержавеющих сталей, находящихся под постоянно действующей нагрузкой. [24]
В качестве катализаторов применяются при этом солянокислые растворы хлористых металлов, например водный раствор, содержащий 10 % - ную соляную кислоту и сулему. [25]
Хлористый алюминий можно получать электролизом хлористого цинка или другого хлористого металла в присутствии угля и глинозема, при этом хлор в момент своего образования действует на глинозем; получается хлористый алюминий, содержащий, возможно, небольшое количество хлористого цинка. [26]
Бессон [121 ] первым стал изучать действие окислов азота на хлористые металлы: он открыл, что они соединяются с многими хлористыми металлами, в том числе и с хлористым алюминием. Он нашел, что соединение хлористого алюминия с окисью азота является более стойким, чем соединение с двуокисью азота. Оба соединения разлагаются водой. [27]
Такое же вещество получается каждый раз, когда какой-либо хлористый металл нагревается в присутствии хромовой и серной кислот. Образования этого летучего вещества легко замечается по тому бурому цвету, который свойствен его парам. Сгущая пары в сухом приемнике, получают жидкость, имеющую уд вес 1 9, кипящую при 118; плотность плра 78, что и соответствует формуле. О, потому это вещество может действовать единовременно и как сильное окисляющее, и как хлорирующее вещество. Приведенное в соприкосновение с горючими веществами, оно их часто воспламеняет; напр. Влагу воздуха притягивает с большою энергией) и потому должно быть сохраняемо в запаянных сосудах. Весьма замечательна большая аналогия физических свойств СгО3С1а и SO2C12, хотя 5ОЙ - тело газообразное, а СгО3 - вещество твердое и нелетучее. [28]
Крюс ( 1893) пользуется дробным осаждением спиртовых растворов хлористых металлов при помощи раствора амилена и этим путем отделяет, напр. [29]
Например, Менделеев обнаружил, что для слабых растворов хлористых металлов, имеющих состав RC1 тН2О, плотность постепенно возрастает вместе с молекулярным весом. Указанной правильностью - как отмечает Менделеев - можно пользоваться при определении веса атома металлов. Но, как показывает далее Менделеев, в обоих случаях молекулярный раствор хлористого бериллия не мог бы встать между удельными весами соответственных растворов других хлористых солей. Я думаю, поэтому, что изучение плотности растворов должно послужить новым средством для установки величины атомного веса элементов [ 12, стр. [30]
Страницы: 1 2 3 4