Образовавшийся аммиак
Cтраница 3
Реакционную смесь разбавляют, восстанавливают восстановленным железом ( Ferrum reductum), а образовавшийся аммиак отгоняют и определяют объемным: методом. [31]
Очень небольшой выход аммиака затрудняет нахождение зависимости между условиями проведения процесса и массой образовавшегося аммиака. Наиболее вероятно установление зависимости между температурой реакции и выходом аммиака при постоянной объемной скорости газов. В этом случае после проведения опыта закрывают кран 7, замечают объем израсходованного азота, меняют приемник 26 и при следующей заданной преподавателем температуре проводят синтез аммиака, как описано выше. [32]
Для использования непрореагировавшей азотоводородной смеси нужно возвращать ее в контактный аппарат после удале-шия образовавшегося аммиака и восполнения прореагировавшей части. Таким образом создается циркуляция газа. [33]
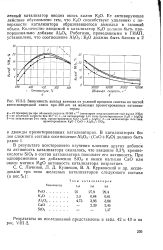 |
Зависимость выхода аммиака от условий процесса синтеза из чистой азото-водородной смеси при 300 am на железных промотированных катализа. [34] |
Ее активирующее действие обусловлено тем, что КгО способствует удалению с поверхности катализатора образовавшегося аммиака в газовый объем. [35]
Она охлаждается, проходя по трубкам водяного конденсатора 1, при этом часть образовавшегося аммиака конденсируется. Газ, охлажденный до 25 - 35 С, проходит сепаратор 6, где сконденсировавшийся аммиак отделяют Ч) т газа, дросселируют до 1 6 МПа и сливают в сбор ник жидкого аммиака 7, а из него направляют на склад аммиака. [36]
Регенерация аммиака состоит в разложении хлористого аммония известковым молоком с последующей отгонкой паром образовавшегося аммиака. Жидкость, представляющая собой в основном раствор СаС12 и не вошедшего в реакцию NaCl, откачивается в отброс. [37]
На практике стремятся работать на предельно допустимом давлении в системе, при хорошей конденсации образовавшегося аммиака, оптимальных температуре и объемной скорости. [38]
Установка синтеза аммиака под давлением 1000 ат предусматривает четыре последовательно соединенных контактных аппарата с выделением образовавшегося аммиака в промежутках между ними. [39]
Синтез аммиака является типичным циклическим процессом, позволяющим непрореагировавшую азотоводородную смесь снова возвращать в производство после выделения из нее образовавшегося аммиака. [40]
Образцы подвергают пиролизу в атмосфере водорода, газы пропускают над тонко измельченным железным катализатором при температуре 400 С [45] и образовавшийся аммиак титруют в сосуде для поглощения. Для этого особенно пригоден иодометрический метод [45], который был разработан для больших образцов и который в применении к малым образцам дает стандартное отклонение 4 нг азота. [41]
Этот же реагент применяют для окисления аминоспиртов и аминокислот в растворах NaOH, причем после окисления названных веществ определяют количество образовавшегося аммиака. [42]
Так как из-за обратимости реакции и недостижения равновесных условий азото-водородная смесь неполностью перерабатывается в аммиак, то после выделения из нее образовавшегося аммиака она снова возвращается на контактирование, циркулируя в замкнутом цикле. [43]
Образовавшийся аммиак отделяют от непрореагировавших азота и водорода, которые после добавления свежей порции азото-водородной смеси в количестве, соответствующем количеству образовавшегося аммиака ( плюс потери от продувки и др.), снова возвращают в цикл. Таким образом осуществляется циклический процесс с циркуляцией азото-водородной смеси. [44]
Так как из-за обратимости реакции и недостижения равновесных условий азото-водородная смесь неполностью перерабатывается в аммиак, то после выделения из нее образовавшегося аммиака она снова возвращается на контактирование, циркулируя в замкнутом цикле. [45]
Страницы: 1 2 3 4