Метод - потенциометрическое титрование
Cтраница 2
Метод потенциометрического титрования оказался чрезвычайно плодотворным при изучении ряда процессов, происходящих в коллоидных системах, таких, как коагуляция и обменная адсорбция, поскольку он позволяет измерять концентрацию ионов в коллоидных растворах, оставляя ее неизменной в процессе измерения. [16]
Метод потенциометрического титрования оказывается особенно полезным при изучении интенсивно окрашенных систем, которые нельзя анализировать при помощи обычных визуальных индикаторов, а также при титровании в неводных средах. Метод является эффективным средством изучения систем, в которых наблюдается заметное взаимодействие продуктов реакции с растворителем, и систем, для которых не удается подобрать внутренний индикатор. При помощи потенциометрического титрования удается также оценить пригодность того или иного визуального индикатора для разрабатываемых методик анализа. [17]
Метод потенциометрического титрования основан на изменении потенциала в процессе титрования. Этот метод позволяет определять органические кислоты, рН растворов, изучать растворимость различных осадков. [18]
Метод потенциометрического титрования основан на измерении величины электрохимического потенциала индикаторного электрода, погруженного в титруемый раствор. Методы потенциометрического анализа начали развиваться с 1892 г. В процессе потенциометрического титрования в зависимости от концентрации титрующего раствора изменяется потенциал индикаторного электрода, измеряемый в вольтах или милливольтах. Потенциал индикаторного электрода может быть измерен только по отношению к другому вспомогательному электроду сравнения. Индикаторный электрод в методе потенциометрического титрования заменяет цветной индикатор, применяемый в обычном методе объемного анализа. Потенциометрическое титрование основано на резком изменении вблизи эквивалентной точки величины электрического потенциала индикаторного электрода. [19]
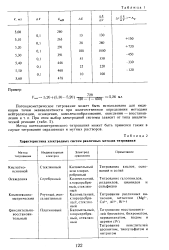 |
Характеристика электродных систем различных методов титрования. [20] |
Метод потенциометрического титрования может быть применен также в случае титрования окрашенных и мутных растворов. [21]
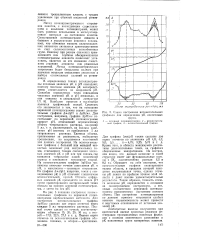 |
Схема построения вспомогательных. [22] |
Метод потенциометрического титрования ионнтов, с последующим соцвставле-нием и анализом потенциограмй, может быть успешно использован в эксплуатационном контроле за состоянием ионитов. Сопоставление потенциограмм свежего и бывшего в эксплуатации анионита показывает, что обменная емкость сильнокислотных анионитов снижается преимущественно за счет сильноосновных ионообменных групп. Поэтому при резком снижении крем-неемкости или глубины обескремнивания потенциограммы анионита позволяют установить, является ли это снижение следствием старения анионита или режимных нарушений. Метод потенциометрического титрования будет безусловно полезен при изучении вопросов отравления анионнтов и выбора оптимальных условий их регенерации. [23]
Метод потенциометрического титрования урана ( IV) сульфатом церия ( IV) использован для определения урана в металлическом цирконии [919] и его сплаве с ураном. После разложения образца циркония уран ( VI) восстанавливают в солянокислом растворе на свинцовом редукторе, добавляют раствор соли Fe ( Ш) и образующееся при этом Fe ( II) титруют потенциометрически стандартным раствором Ce ( SO4) 2, используя платиновый индикаторный электрод. [24]
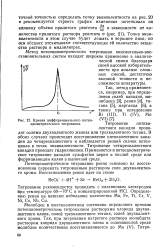 |
Кривая дифференциального потен - ( [ г. [25] |
Метод потенциометрического титрования окислительно-восстановительных систем находит широкое применение в аналитической химии благодаря своей высокой избирательности при анализе сложных смесей, достаточно высокой точности и несложности аппаратуры. [26]
Методом потенциометрического титрования были определены константы ионизации соединения III a - а-и в водно-метанольном ( 2 5 % - ном) растворе и соединений II а-н, р-т ( табл. 1) в 50 % - ном водном ацетоне. Провести определение рКа соединений III a - и и II а-н, р-т в одинаковых условиях не удалось, поскольку препараты II а-н, р-т не растворяются в водно-метанольной 2 5 % - ной смеси, а вещества III а-и в 50 % - ном ацетоне являются слишком слабыми кислотами. Последнее было доказано определением константы ионизации соединения III а-самой сильной из этого ряда кислот - в 50 % - ном водном ацетоне. Определить рКа соединений II о, п не удалось ввиду гидролиза этих продуктов в условиях опыта. [27]
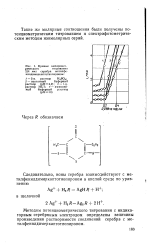 |
Кривые амперомет-рического титрования. [28] |
Методом потенциометрического титрования с индикаторным серебряным электродом определены величины произведения растворимости соединений серебра с ме-тилфенилдимеркаптотиопироном. [29]
 |
Влияние значения рН на емкость битумных катионитов СБН ( 1 - 3 и СБТ. (. - 3 по ионам стронция ( 1, 1, цезия ( 2, 2 и натрия ( 3, 3. [30] |
Страницы: 1 2 3 4