Метод - эдман
Cтраница 2
Для определения аминокислотной последовательности рибосомальный белок L32 был расщеплен на фрагменты двумя различными методами ( А, Б) и для полученных фрагментов методом Эдмана была определена первичная структура. [16]
Аминокислотный анализ показал, что полипептид состоит из остатков следующих аминокислот: глицина, аланина, валина, лейцина ( изолейцина), серина, треонина, аспарагиновой и глутаминовой кислот, аргинина, лизина и гистидина, а N-концевой аминокислотой, как это удалось установить с помощью метода Эдмана, является аспарагин. [17]
Эту процедуру ступенчатого расщепления пептида с N-конца можно повторять многократно, идентифицируя последовательно одну аминокислоту за другой. Метод Эдмана используется в качестве химической основы для определения первичной структуры белков и пептидов. Он реализован в специальном приборе-секвенаторе ( от англ, sequence - последовательность), работающем в автоматическом режиме и позволяющем определить последовательность аминокислот с N-конца пептида до 50 - 60 аминокислотных остатков. [18]
Исследование концевых аминокислот в белках и пептидах играет важную роль в изучении как химической структуры, так и специфических биологических свойств этих соединений. Для определения N-кон-цевых аминокислот широко используются динитрофторбензольный метод Сэнгера, фенилизотиоцианатный ( метилизотиоцианатный) метод Эдмана и дансильный метод Грэя и Хартли. [19]
Само секвенированяе не имеет прямого отношения к хроматографии, поскольку опо представляет собой способ автоматизации проведения определенной химической реакции, и не более того. Однако продукты этой реакции идентифицируются исключительно методами хроматографии, а само секвенирование белков играет столь важную роль в молекулярной биологии, что необходимо хотя бы в общих чертах познакомить читателя с методом Эдмана и принципом устройства секвенаторов; это ознакомление вынесено в конец книги - см. прил. [20]
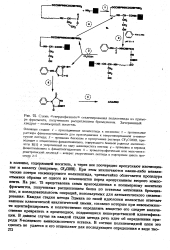 |
Схема твердофазного секвенирования полипептида на примере фрагмента, полученного расщеплением бромцианом. Зачерненный квадрат - полимерный носитель. [21] |
При этом исключаются какие-либо механические потери секвенируемого полипептида, чрезвычайно облегчается процедура отмывки образца от одного из компонентов перед пропусканием второго компонента. На рис. 75 представлена схема присоединения к полимерному носителю фрагментов, полученных расщеплением белка по остаткам метионина бромцианом, и последовательность операций, используемых для автоматического секвенирования. Каждая стадия метода Эдмана по своей идеологии полностью отвечает канонам классической аналитической химии, согласно которым при невозможности идентифицировать и количественно определить вещество его следует количественно превратить в производное, поддающееся непосредственной идентификации. В данном случае на каждой стадии метода речь идет об определении природы N-концевого аминокислотного остатка. [22]
В результате гидролиза в разных условиях получается набор полипептидных осколков, которые разделяют хроматографическими методами, разработанными Мартином и Синджем. Последовательность связей аминокислот в каждом из полипептидных осколков может быть установлена приведенными выше методами, например методом Эдмана. [23]
Расщепление полипептидной цепи на фрагменты проводят обычно при помощи протеолитических ферментов, таких, как трипсин, химотрипсин или пепсин. Эти ферменты действуют на различные участки полипептидной цепи, так как имеют повышенное сродство к различным аминокислотным остаткам. Оказалось, что трипсин гидролизует только те пептидные связи, в образовании которых участвует карбоксильная группа лизина или аргинина, а химотрипсин гидролизует связи по фенилаланину, триптофану и тирозину. Обычно протеолитические ферменты, гидролизующие полипептидные цепи, предварительно иммобилизуют на нерастворимых матрицах для более легкого отделения их от продуктов гидролиза. Далее определяют аминокислотные последовательности каждого полипептидного фрагмента. Для этого чаще всего используют метод Эдмана, заключающийся в анализе полипептида только с TV-конца. Концевая аминокислота при взаимодействии с фенилизотиоцианатом в щелочной среде образует стойкое соединение, которое можно отщепить от полипептида без его деградации. Фенилтиогидантоиновое ( ФТГ) производное аминокислоты идентифицируется хроматографическим методом. [24]
Сэнджер существенно облегчил себе задачу тем, что использовал частичный кислотный гидролиз для расщепления двух цепей, ин - сулина на достаточно малые фрагменты, которые уже можно было охарактеризовать с помощью имеющейся техники. Несмотря на то, что эти две цепи содержат лишь 21 и 30 остатков аминокислот соответственно, в результате гидролиза образовалось много фрагментов и объем экспериментальной работы, включая их разделение, идентификацию и определение последовательности, занял у Сэнд-жера несколько лет; за эту работу ему была присуждена Нобелевская премия. С помощью современной техники эту же работу можно осуществить, самое большое, за несколько недель. Современная стратегия состоит в расщеплении белков на небольшое число относительно крупных фрагментов, что можно осуществить либо химически ( см. раздел 23.3.5), либо ферментативно ( см. разд. Использование более одного метода расщепления обычно приводит к различным фрагментам, последовательности которых перекрываются. Если же начальные фрагменты достаточно малы, то последовательность можно определить без дополнительных реакций расщепления. Такого рода стратегия удается благодаря наличию нескольких совершенных методов разделения пептидов н тому, что с помощью метода Эдмана можно провести около 40 стадий последовательного расщепления полипептида. [25]
Страницы: 1 2