Дюгема
Cтраница 2
Согласно уравнению Дюгема - Маргулеса, сумма первых двух членов правой части этого уравнения равна нулю. [16]
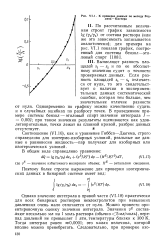 |
К проверке данных по методу Ред-лиха - Кистера. [17] |
Гиббса - Дюгема, строго справедливо для изотермо-изобарных условий, реальные же данные о равновесии жидкость - пар получают для изобарных или изотермических условий. [18]
Из правила Дюгема - Маргулеса1 следует, что если изотерма парциальной упругости пара одного из компонентов прямая, то при той же температуре изотерма второго компонента также прямая. [19]
Согласно уравнению Дюгема - Маргулеса, сумма первых двух членов правой части этого уравнения равна нулю. [20]
По теореме Дюгема полная вариантность закрытой системы равна двум, и любое состояние системы определяется однозначно, если известны исходные массы компонентов. [21]
Согласно уравнению Дюгема - Маргулеса, сумма первых двух членов правой части этого уравнения равна нулю. [22]
Гиббса - Дюгема ( 41) и условие Л Л N-B jVc 1) не позволяют найти три неизвестные мольные доли. Для того чтобы преодолеть возникшее затруднение, нужно найти третье независимое уравнение, связывающее между собой мольные доли компонентов в конденсированной фазе. Таким дополнительным условием, по-видимому, может быть уравнение линии дистилляции. [23]
По теории Дюгема гигротермическое равновесие наступает медленно, поэтому наблюдаемое равновесие не является истинным. Таким образом, в процесс сорбции получаем равновесное влагосодержание меньше истинного, а в процесе десорбции, - наоборот, несколько больше истинного. [24]
Гиббса - Дюгема, широко используемое в теории растворов. [25]
Гиббса - Дюгема, а в каждом из уравнений Гиббса - Дюгема имеется / г 2 переменных. Поэтому при определении f необходимо учитывать любые уравнения связи между переменными, описывающими состояние системы. Например, если рассмотреть многофазную систему, в которой осуществляются химические превращения, это приведет к необходимости учитывать также число уравнений, описывающих химические равновесия. [26]
Гиббса - Дюгема для гомогенной системы, где адсорбент фигурирует в качестве одного из компонентов. [27]
Эту истинность Дюгем никогда не отнимет у физических теорем: они представляют собой описание реального. [28]
Уравнение Гиббса - Дюгема (1.24.12) служит свидетельством линейной зависимости между градиентами обобщенных потенциалов. Перечень примеров может быть продолжен. [29]
Конечно, теорема Дюгема не противоречит правилу фаз. Следует иметь в виду, что при обсуждении закрытых систем вкладывается несколько другой смысл в понятия вариантности и переменных состояния, чем при начальном выводе правила фаз. [30]
Страницы: 1 2 3 4