Дюлонг
Cтраница 3
Правило Дюлонга и Пти справедливо при 15 - 25 С. С понижением температуры произведение А С уменьшается. [31]
Закон Дюлонга и Пти является, как мы видели, следствием закона равномерного распределения энергии по степеням свободы. Поэтому тот факт, что твердые тела в действительности не следуют закону Дюлонга и Пти при низких температурах, показывает, что гипотеза о равномерном распределении энергии по степеням свободы является приближением. [32]
Закон Дюлонга и Пти приблизительно верен для ряда веществ. [33]
Закон Дюлонга и Пти сравнительно хорошо подтверждается на опыте при не слишком низких температурах. [34]
Закон Дюлонга и Пти, однако, не выполняется при низких, а для ряда веществ ( бор, алмаз, кремний) и при средних температурах. [35]
Правило Дюлонга и Пти можно вывести теоретически при классическом описании колебаний атомов. Будем рассматривать кристалл, состоящий из N атомов, которые участвуют - преимущественно в колебательном движении. [36]
Закон Дюлонга и Пти является, как мы видели, следствием закона равномерного распределения энергии по степеням свободы. Поэтому тот факт, что твердые тела в действительности не следуют закону Дюлонга и Пти при низких температурах, показывает, что гипотеза о равномерном распределении энергии по степеням свободы является приближением. [37]
Правило Дюлонга и Пти соблюдается для твердых одноатомных тел при достаточно высоких температурах. Для большинства тел такой достаточно высокой температурой является уже комнатная температура. Однако для некоторых тел с малым атомным весом, например для бериллия, бора, углерода ( алмаза), комнатная температура недостаточно высока, и они подчиняются правилу Дюлонга и Пти лишь при более высокой температуре. Наоборот, при охлаждении все тела обнаруживают отступления от правила Дюлонга и Пти. При охлаждении удельная теплоемкость всех тел уменьшается. [38]
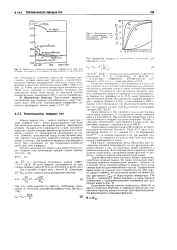 |
Иямомснис плотности различных модификаций SiO. при нагреве, охлаждении и в процессах превращения по данным.| Зависимость атомных тенлоемкостей при постоянном объеме от температуры. [39] |
Закон Дюлонга и Пти применим только при температурах выше комнатных, но оказывается иногда неверным даже и в этой области. При понижении температуры удельная теплоемкость твердых тел резко возрастает. На рис. 1 показаны теплоемкости, приходящиеся на один атом, для некоторых веществ в диапазоне от 0 до 400 К. [40]
Правило Дюлонга и Пти соблюдается для твердых одноатомных тел при достаточно высоких температурах. Для большинства тел такой достаточно высокой температурой является уже комнатная температура. Однако для некоторых тел с малым атомным весом, например для бериллия, бора, углерода ( алмаза), комнатная температура недостаточно высока, и они подчиняются правилу Дюлонга и Пти лишь при более высокой температуре. Наоборот, при охлаждении все тела обнаруживают отступления от правила Дюлонга и Пти. При охлаждении удельная теплоемкость всех тел уменьшается. [41]
Правило Дюлонга и Пти соблюдается для твердых одноатомных тел при достаточно высоких температурах. Для большинства тел такой достаточно высокой температурой является уже комнатная температура. Однако для некоторых тел с малым атомным весом, например для бериллия, бора, углерода ( алмаза), комнатная температура недостаточно высока, и они подчиняются правилу Дюлонга и Пти лишь при более высокой температуре. Наоборот, при охлаждении все тела обнаруживают отступления от правила Дюлонга и Пти. При охлаждении удельная ( теплоемкость всех тел уменьшается. [42]
Правило Дюлонга и Пти вытекает из экспериментальных наблюдений. Позже это правило было выведено и на основании кинетической теории. В кристалле атомы колеблются вокруг определенных положений равновесия. Энергия этих движений составляет часть внутренней энергии кристалла. Эта энергия состоит из кинетической энергии, за счет которой атомы смещаются из состояния равновесия, и потенциальной энергии, за счет которой каждый атом возвращается в состояние равновесия. Согласно Больцману, можно доказать, что эти энергии равны. Поскольку кинетическая энергия атомов, содержащихся в 1 г-атоме кристаллического вещества, такая же, как для газов, а именно 3 / 2 RT ( см. стр. [43]
Формула Дюлонга дает, вообще говоря, не особенно точные результаты ( от 1 4 до 11 9 %), менделеевская в этом отношении точнее, по она менее применима для нефти, чем для углей. Все формулы дают между собой более или менее сходные результаты, уклоняющиеся однако от эмпирически найденной величины. Разница объясняется различием внутреннего строения углеводородов. Кроме того на результат вычисления должна влиять как. [44]
Закон Дюлонга и Пти, как это и следовало ожидать, вскоре после открытия был применен для проверки атомных весов элементов. Это был существен - - ный шаг в развитии атомного учения: исправление атомных весов осуществлялось путем подбора коэффициентов, на которые надо умножить экспериментально найденные данные, чтобы получить правильные величины атомных весов. [45]
Страницы: 1 2 3 4