Флуоресцентный метод
Cтраница 1
Флуоресцентный метод, или флуориметрия, основан на измерении интенсивности света, испускаемого веществом под воздействием падающих на него ультрафиолетовых лучей. [1]
Флуоресцентный метод позволяет обнаружить глубокие трещины, светящиеся в виде широких полос, и тонкие трещины, а также и MHS кроскопические, которые светятся тонкими линиями. [2]
Флуоресцентный метод пока не получил сколько-нибудь заметного применения в силу ряда ограничений, но некоторые его варианты показывают быстрое развитие, благодаря сравнительной простоте и достаточно высокой чувствительности. [3]
Флуоресцентный метод применен для определения бора, причем в качестве реагента как для качественного, так и для количественного определения используют бензоин. [4]
Флуоресцентный метод ( А) особенно пригоден для определения урана, присутствующего при низких концентрациях, так как точность определения в среднем составляет примерно 5V, метод можно применять для определения вплоть до 0 1 % урана, беря на анализ небольшие аликвотные части раствора анализируемого образца; указанная точность достижима в том случае, если отделить мешающие элементы или устранить вызываемые ими помехи, предприняв соответствующие меры. [5]
Флуоресцентный метод более чувствителен, чем спектрофотометри-ческий. Определяемые концентрации 0 005 - 0 5 мкг Ga / Ю мл ( лампа СВДШ-250); наиболее удобны для сравнения концентрации 0 01 - 0 05 мкг Ga / Ю мл. Ошибка определения не превышает 20 отй. [7]
Флуоресцентный метод применяют для изучения быстрых реакций возбужденных молекул, кислотно-основных реакций возбужденных молекул и комплексообразования в возбужденном электронном состоянии, определения концентрации люминесцирующих веществ в смеси, изучения кинетики и механизма ферментативных реакций, изучения межмолекулярного переноса энергии. [8]
Флуоресцентный метод применяют для изучения быстрых реакций возбужденных молекул, кислотно-основных реакций возбужденных молекул и комплек-сообразования в возбужденном электронном состоянии, определения концентрации люминесцирующих веществ в смеси, изучения кинетики и механизма ферментативных реакций, изучения межмолекулярного переноса энергии. [9]
 |
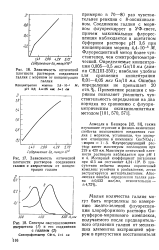
Спектральные кривые поглощения ( / и флуоресценции ( 2 для некоторых веществ. [10] |
Флуоресцентный метод может быть использован для прямого и косвенного анализа. В первом случае для анализа используется непосредственно флуоресценция исследуемого объекта. Следует заметить, что среди неорганических веществ очень мало веществ, способных флуоресцировать самостоятельно. К числу таких веществ относятся соединения урана и редкоземельных элементов - церия, европия, самария и др. Значительно чаще встречаются флуоресцирующие органические вещества, например резорцин, хинин, морфин и многие другие. Для большинства неорганических ионов применение флуоресцентного метода связано с образованием флуоресцирующих соединений с различными органическими веществами. [11]
Флуоресцентный метод позволяет определять минимальные количества урана: применяя сухой метод, можно определить пр помощи фотоэлектрического флуорометра 0 0001 ( одну десятитысячную) мкг урана. Процесс заключается в следующем: исследуемый раствор соли урана в количестве 0 005 - 0 1 мл помещают пипеткой в платиновую чашечку и выпаривают на специальной лампе. К сухому остатку добавляют 0 3 г смеси фторида натрия с содой и сплавляют на газовой горелке. После охлаждения сплавленный диск соли облучают ртутной лампой и возникшую при этом желто-зеленую флуоресценцию измеряют специальным прибором. Количество урана определяется с помощью-калибровочной кривой. [12]
 |
Упрощенная диаграмма энергетических уровней. [13] |
Флуоресцентный метод применяют для изучения быстрых реакций возбужденных молекул, кислотно-основных реакций возбужденных молекул и комплексообразования в возбужденном электронном состоянии, определения концентрации люминесцирующих веществ в смеси, изучения кинетики и механизма ферментативных реакций, изучения межмолекулярного переноса энергии. [14]
Флуоресцентный метод особенно удобен для качественного анализа. Чувствительность всех методов лежит в интервале 0.5 - 2 мкг / мл конечного раствора. [15]
Страницы: 1 2 3 4