Флуоресцентный метод
Cтраница 3
Применение флуоресцентного метода позволяет контролировать качество углей с переменным составом золы при использовании криогенного охлаждения полупроводникового детектора, вакуумирования зоны измерения. Аппаратура дорогостояща и сложна. [31]
Чувствительность флуоресцентного метода определения корала лимитируется величиной флуоресценции растворов, полученных при анализе необработанных коралом образцов. В случае анализа образцов жира или мяса чувствительность метода составляет 0 02 мкг / кг корала. Метод дает возможность открывать в животной ткани от 80 до 100 % корала и от 100 до 110 % его кислородного аналога. [32]
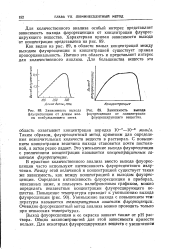 |
Зависимость выхода флуоресценции от длины волны возбуждающего света. [33] |
Таким образом флуоресцентный метод применим для определения незначительных количеств веществ в растворах. С повышением концентрации величина выхода становится почти постоянной, а затем резко падает. Это уменьшение выхода флуоресценции с увеличением концентрации называется концентрационным гашением флуоресценции. [34]
В принципе флуоресцентный метод должен рассматриваться как метод локального зондирования, поскольку исследуется только область, находящаяся на пересечении возбуждающего луча и оптического пути детектора. Выбранный флуоресцирующий объем был равен приблизительно. [35]
Важным достоинством флуоресцентных методов является их чувствительность к фотохимическим, окислительным и другим процессам химической деградации углеводородов, которые интенсивно происходят при разливах нефти. [36]
Главным преимуществом флуоресцентных методов является их высокая чувствительность - в большинстве систем определяются концентрации около 0 01 ррт. При наличии хороших приборов можно достигнуть воспроизводимость 1 %, но для того чтобы добиться правильности такого же порядка, необходимо обращать особое внимание на ряд деталей и исключить все возможные источники ошибок. Таких источников довольно много. Например, если интенсивность флуоресценции сильно зависит от рН, необходимо ввести буфер с соблюдением ряда предосторожностей. В других системах интенсивность излучения может изменяться со временем вследствие фотохимического разложения флуоресцирующих молекул. [37]
Принципиальным преимуществом флуоресцентных методов является низкий уровень шума. На практике большинство сорбентов флуоресцирует в той пли иной степени, однако связанные с этим помехи ниже оптического шума, возникающего при измерении величины пропускания и отражения. Это делает флуоресцентные ( все выше сказанное не распространяется на метод гашения флуоресценции) методы более перспективными, чем фотометрические, в связи с их простотой и отсутствием сложного оборудования. [38]
В основу флуоресцентного метода определения концентрации SO2 положена независимость спектра флуоресценции от длины волны возбуждающего излучения. Экспериментально это выражается в следующем. Флуоресценция возникает от того, возбуждаются ли молекулы ( атомы, ионы) анализируемого вещества излучением, спектр которого находится в интервале длин волн Xi... Одновременно абсолютная погрешность флуоресценции зависит от того, производится ли возбуждение в максимуме полосы поглощения или на ее крыльях. [39]
При определении флуоресцентным методом используют оксин. При определений флуоресцентным методом используют морин. При определении флуоресцентным методом используют бензоин. При определении флуоресцентным методом используют кверцетин. [40]
Скополамин определяют количественно флуоресцентным методом [93], скополамин и гиосциамин [94] - прямым денсито-метрическим методом. [41]
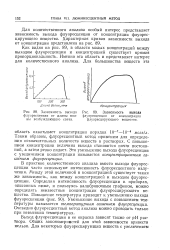 |
Зависимость выхода [ IMAGE ] 89. Зависимость выхода. [42] |
Таким образом, флуоресцентный метод применим для определения незначительных количеств веществ в растворах. С повышением концентрации величина выхода становится почти постоянной, а затем резко падает. Это уменьшение выхода флуоресценции с увеличением концентрации называется концентрационным гашением флуоресценции. [43]
Чрезвычайно высокая чувствительность флуоресцентного метода позволяет применять его для изучения свойств самих ферментов и их комплексов с субстратом и коферментом. При измерении, например, констант диссоциации и констант Михаэлиса для комплексов фермент - субстрат или фермент - кофермент спектрофотометрия и другие методы оказываются часто недостаточно чувствительными. Когда субстрат флуоресцирует, можно определять константы Михаэлиса на несколько порядков меньше, чем спектрофото-метрическим методом. [44]
Единственный серьезный недостаток флуоресцентного метода определения урана заключается в том, что значительное число элементов может гасить флуоресценцию урана, что приводит к ошибочным результатам. Элементы, которые гасят флуоресценцию урана, можно классифицировать следующим образом1: сильногасящие ( 1 - 10 у такого элемента уменьшают флуоресценцию урана на 10 % и более): Cr, Mn, Co, Ni, Ag, Au, Pt, Pb, La, Ce, Pr, Nd; умеренногасящие ( 10 - 50 у уменьшают флуоресценцию урана на 10 %): Fe, Cu, Zn, Sn, Th; слабогасящие ( 50 - 1000 у уменьшают флуоресценцию урана на 10 %): Ti, W. Приводимые данные относятся к 2 г флюса смеси фторида, карбоната натрия и карбоната калия. [45]
Страницы: 1 2 3 4