Термогравиметрический метод
Cтраница 1
Термогравиметрический метод является наиболее распространенным благодаря его простоте и универсальности. [1]
Термогравиметрический метод основан на взвешивании пробы исследуемого вещества до и после высушивания ( центрифугирования) до постоянной кассы. [2]
Термогравиметрический метод определения наполнителей, разложение которых сопровождается характерным экзо - или эндотермическим эффектом, также нашел применение для количественного анализа. Этот метод не требует обязательного предварительного разделения минеральной части полимера. [3]
Термогравиметрический метод определения термической стабильности полимеров является относительным, но результаты его-хорошо согласуются с методами, основанными на непосредственном измерении потерь эксплуатационных свойств. [4]
Термогравиметрическим методом изучена термическая устойчивость гексагалогентеллуратов таллия. [5]
Термогравиметрическим методом определены температуры дегидратации и разложения полученных комплексов. [6]
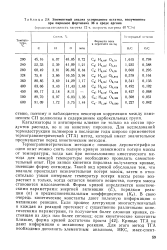 |
Элементный анализ углеродного остатка, полученного при пиролизе фортизана 36 в среде аргона. [7] |
Термогравиметрическим методом с помощью дериватографа за один опыт можно снять полную кривую зависимости потери массы от температуры, тогда как при использовании кинетического метода для каждой температуры необходимо проводить самостоятельный опыт. При записи кинетики пиролиза получаются кривые, имеющие форму сигмоиды. Такой вид кривой обусловлен тем, что вначале происходит незначительная потеря массы, затем в относительно узком интервале температур потеря массы резко возрастает и только, когда остается немного вещества, потеря массы становится малозаметной. [8]
Комплексным термогравиметрическим методом показана неравноценность связей соль - вода. [9]
Изучение термогравиметрическим методом [28] ЭДТА, комплексо-на III, ( трилона Б), диаммонийной соли ЭДТА, этилендиаминтетраце-татов железа, меди, кальция, магния и кобальта, цитратов железа и меди в твердом виде показало, что разложение всех этих соединений происходит при 200 С и выше. Комплексен III и этилендиамин-тетрацетат железа в растворе начинают распадаться [28] при температуре около 150 С. Полностью процесс разложения заканчивается при 270 С с образованием в качестве конечного продукта, по данным рентгенографического анализа, магнетита. Полученные таким образом результаты указывают на применимость данных соединений для отмывки и пассивации, проводимых соответственно при 100 - 150 и 270 С. [10]
Изучение термогравиметрическим методом [28] ЭДТА, комплексо-на Ш ( трилонаБ), диаммонийной соли ЭДТА, этилендиаминтетраце-татов железа, меди, кальция, магния и кобальта, цитратов железа и меди в твердом виде показало, что разложение всех этих соединений происходит при 200 С и выше. Комплексен III и этилендиамин-тетрацетат железа в растворе начинают распадаться [28] при температуре около 150 С. Полностью процесс разложения заканчивается при 270 С с образованием в качестве конечного продукта, по данным рентгенографического анализа, магнетита. Полученные таким образом результаты указывают на применимость данных соединений для отмывки и пассивации, проводимых соответственно при 100 - 150 и 270 С. [11]
В термогравиметрическом методе можно более точно определить тепловые эффекты. [12]
В термогравиметрическом методе можно наблюдать процессы, которые не наблюдаются при термографическом методе. [13]
Исследования проводили термогравиметрическим методом в изотермических условиях на дериватографе системы Паулик - Паулик, Эрдей в интервале 723 - 1043 К. Объектом исследования служил кокс с частицами среднего размера 100 мкм, полученный в результате пиролиза ОСК с примесями БСК. [14]
Его исследовали термогравиметрическим методом при линейно программированной температуре ( 120 С / час от 25 до 1000) и в изотермических условиях в интервале 400 - 525 в вакууме, азоте или в атмосфере воздуха. В начале деструкции удаляются летучие продукты, по-видимому присутствовавшие в образце. Их количество составляет 2 - 3 % от веса образца. [15]
Страницы: 1 2 3 4