Температурно-кинетический метод
Cтраница 1
Температурно-кинетический метод, как и метод вращающегося диска, не дает ответа на вопрос о том, какой из частных процессов ( анодный или катодный) в большей степенл контролирует скорость цементации; и какая именно. Электрохимический метод основан на сопоставлении частных поляризационных кривых катодного и анодного процессов с областью потенциалов, в которой проходит контактный обмен. [1]
Температурно-кинетический метод С. В. Горбачева с каждым годом все больше применяется при изучении кинетики электроосаждения и электрорастворения металлов. [2]
Применение температурно-кинетического метода при изучении анодного растворения при повышенных плотностях тока алюминиевого сплава показало, что при небольшой величине потенциала преобладают ограничения, обусловленные химической поляризацией. Наибольшее сопротивление транспортированию вещества при этом оказывает, по-видимому, покрывающая анод фазовая пленка с довольно рыхлой структурой. [3]
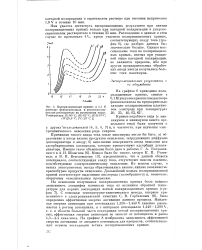 |
Поляризационные кривые в 0 1 М растворе феноксиэтанола в уксусносеэно-кислом растворителе на платиновом аноде. Температура. ( I 80 С. ( II 62 С. ( III 40 С. ( IV255 С. ( V 20 С. f. [4] |
С помощью температурно-кинетического метода, впервые примененного в электрохимической кинетике С. В. Горбачевым [8], была определена эффективная энергия активации данного процесса. На графике 8 изображена зависимость эффективной энергии активации от анодного потенциала для процессов, соответствующих первым восходящим ветвям поляризационных кривых. [5]
Сопоставление закономерностей, выявленных температурно-кинетическим методом и при помощи вращающегося дискового катода, указывает на изменение характера поляризации суммарного электродного процесса в фосфатном растворе с повышением потенциала катода. Так, при потенциалах ветви 7 кривой проявляется совместное влияние концентрационной и химической поляризации. Это подтверждает предположение о влиянии реакции ионизации кислорода и пассивирования поверхности катода на кинетику электродного процесса. [6]
 |
Зависимость эффективной энергии активации от величины катодной поляризации кадмиевого катода. [7] |
Анализ данных, полученных температурно-кинетическим методом, дает основание считать, что общая величина катодной поляризации кадмия в цианистом электролите обусловлена ограничениями как химического, так и концентрационного характера. При малой величине поляризации, примерно до 40 мв, решающую роль играет химическая поляризация, а при более отрицательном потенциале - концентрационная. [8]
Исследование анодного растворения сплава ВК8 температурно-кинетическим методом показало, что при небольшой поляризации ( область минимума поляризационной кривой) главную роль играют кинетические ограничения из-за химической поляризации. По мере изменения значений потенциала в положительную сторону все большее значение приобретают затруднения транспортирования продуктов анодной реакции через нарастающую пленку на аноде. [9]
Существует также принципиальная возможность определения температурно-кинетическим методом энергии активации при торможении процесса на стадии кристаллизации. [10]
В данной работе необходимо исследовать природу поляризации температурно-кинетическим методом. [11]
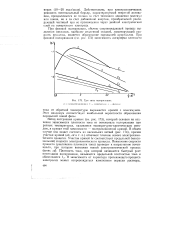 |
Три типа поляризации. [12] |
Метод построения кривых ( см. рис. 173), который основан на изучении зависимости плотности тока от потенциала поляризации при разных температурах, называется температурно-кинетическим методом, а кривая этой зависимости - поляризационной кривой. Участок кривой be соответствует предельной ( максимальной) скорости электрохимического процесса. [13]
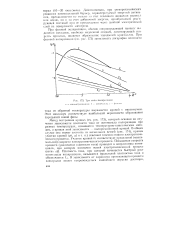 |
Три типа поляри. чацин. [14] |
Метод построения кривых ( см. рис. 173), который основан на изучении зависимости плотности тока от потенциала поляризации при разных температурах, называется температурно-кинетическим методом, а кривая этой зависимости - - поляризационной кривой. Участок кривой be соответствует предельной ( максимальной) скорости электрохимического процесса. [15]
Страницы: 1 2